Items, objectifs pédagogiques
Item 253 – Obésité de l’enfant et de l’adulte (voir item 71)
- Diagnostiquer une obésité de l’enfant et de l’adulte.
- Connaître les principes de la prise en charge thérapeutique.
Item 249 – Modifications thérapeutiques du mode de vie (alimentation et activité physique) chez l’adulte et l’enfant
- Évaluer le comportement alimentaire et diagnostiquer ses différents troubles.
- Argumenter les bénéfices et les effets cliniques de la pratique de l’activité physique.
- Identifier les freins au changement de comportement.
- Savoir prescrire et conseiller en diététique.
- Promouvoir l’activité physique chez le sujet malade (démarche, orientations).
Avant de commencer…
L’obésité de l’enfant implique l’existence d’une prédisposition constitutionnelle, principalement géné-tique. Elle est le plus souvent commune, les obésités secondaires ou syndromiques étant rares, mais il existe un continuum entre obésité commune et obésité monogénique.
Les bases génétiques de l’obésité requièrent encore beaucoup de recherche pour être complètement élucidées.
Sa définition repose sur le calcul de l’IMC et sa comparaison aux normes pour l’âge et le sexe.
Les complications somatiques sont rares durant l’enfance ; les conséquences psychiques sont fré-quentes.
La prise en charge thérapeutique s’inscrit dans le long terme et doit être individualisée.
L’objectif minimal est la stabilisation de l’excès pondéral avec un accompagnement psychosocial centré sur l’enfant et sa famille.
I. Pour bien comprendre
La prévalence du surpoids et de l’obésité en France et dans tous les pays industrialisés est stable depuis le début du siècle chez l’enfant et l’adolescent, autour de 15 à 20 % en France, avec ce-pendant une augmentation pour les situations les plus sévères.
II. Diagnostiquer une obésité de l’enfant
A. Diagnostic positif
L’indice de masse corporelle (IMC) répond à la définition suivante : poids (en kg) rapporté au carré de la taille (en mètre) : IMC = Poids/Taille2.
Le surpoids et l’obésité se définissent chez l’enfant à l’aide des courbes d’IMC, différentes selon le sexe. On ne peut donc appliquer des seuils fixes comme chez l’adulte. Le tableau 16.1 présente les définitions du surpoids et de l’obésité.
Tableau 16.1. ![]() Définitions du surpoids et de l’obésité.
Définitions du surpoids et de l’obésité.
| Surpoids | En France : IMC ≥ à la courbe du 97e percentile pour l’âge (équivalent à un IMC adulte de 26 kg/m2) La définition internationale utilise la courbe équivalente à un IMC adulte de 25 kg/m2 |
| Obésité | IMC ≥ à la courbe équivalente à un IMC adulte de 30 kg/m2 Les définitions françaises et internationales sont identiques |
Un calcul régulier de l’IMC fondé sur les mesures régulières du poids et de la taille permet de tracer la courbe d’IMC (fig. 16.1).
L’IMC varie au cours du développement : après une augmentation dans la 1re année de vie, l’IMC diminue pour atteindre un nadir (point le plus bas). La réascension intervenant ensuite est appelée rebond d’adiposité.
Dans la population générale, l’âge moyen physiologique du rebond d’adiposité est de 6 ans. Il est très souvent plus précoce chez l’enfant obèse, et souvent aux alentours de 3 ans.
Un rebond d’adiposité précoce est prédictif d’une obésité future.
B. Diagnostic étiologique
1. Obésité commune
L’obésité dite commune est la cause principale d’obésité de l’enfant.
Elle se traduit par une obésité sans signes associés (dysmorphie, retard mental, retard statural), avec le plus souvent des antécédents familiaux d’obésité.
Une cause psychologique est souvent évoquée (divorce parental, décès familial, stress émotionnel, maltraitance, etc.) mais il s’agit en fait d’un facteur déclenchant sur prédisposition génétique ou aggravant mais non causal.
L’obésité commune est liée à une prédisposition génétique dont l’origine exacte est encore in-complètement élucidée. On retrouve de plus en plus souvent des variants génétiques expliquant l’obésité, même si la majorité d’entre eux restent à découvrir.
2. Obésités d’origine génétique connue
Certaines obésités, syndromiques ou non, ont une origine génétique connue.
Les causes syndromiques souvent associées à un trouble du neurodéveloppement sont à évoquer en cas de retard mental, dysmorphie, retards statural et/ou pubertaire. Les gènes de quelques-uns de ces syndromes ont été identifiés et permettent donc un diagnostic moléculaire.
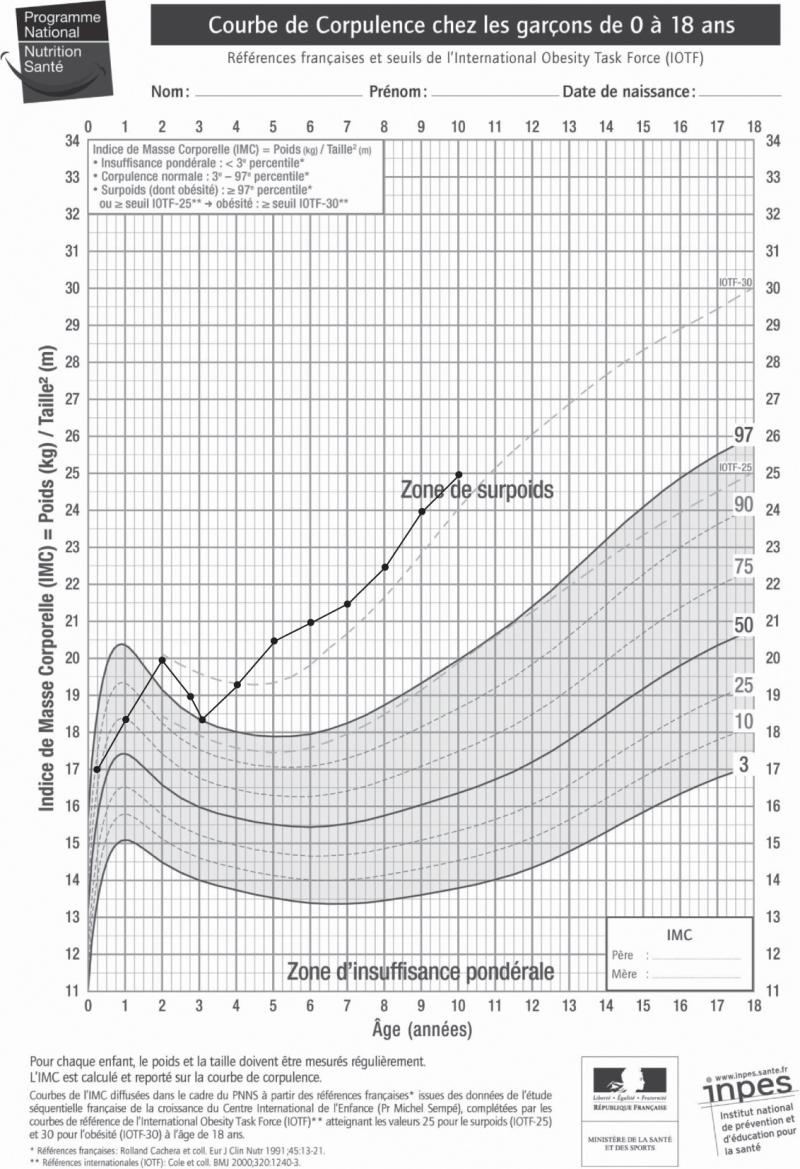
Fig. 16.1. ![]() Courbe d’IMC avec rebond d’adiposité précoce.
Courbe d’IMC avec rebond d’adiposité précoce.
Le terme « zone de surpoids » prête à confusion. Il aurait été préférable de l’appeler « zone de sur-charge pondérale ». Le surpoids correspond à un IMC situé entre le 97e percentile et l’IOTF 30 et l’obésité à un IMC supérieur à l’IOTF 30.
Les plus connus sont le syndrome de Prader-Willi (associant hypotonie néonatale avec difficultés de succion et de prise de poids suivi par une obésité précoce avec hyperphagie intense après la période infantile, dysmorphie faciale, acromicrie – défaut de développement en longueur des membres –, retard statural, hypogonadisme, retard des acquisitions, et troubles du comporte-ment) et le syndrome de Bardet-Biedl (retard des acquisitions, rétinite pigmentaire, anomalies rénales, hypogonadisme, polydactylie).
Les autres causes monogéniques connues sont à évoquer en cas d’obésité précoce (avant 2 ans) et le plus souvent sévère, avec hyperphagie intense et souvent associée à des anomalies endocriniennes (hypogonadisme, insuffisance surrénale).
Des mutations sur les gènes de la voie leptine/mélanocortines qui régulent la prise alimentaire au niveau hypothalamique ont été identifiées. D’autres mutations devraient être trouvées dans le futur, notamment dans les formes les plus sévères d’obésité.
La prescription d’analyses génétiques n’est pas faite en routine mais par des centres spécialisés.
3. Obésités d’origine endocrinienne
Les obésités d’origine endocrinienne sont rares.
Il serait préférable de les définir comme un diagnostic différentiel de l’obésité commune ou d’origine génétique connue plutôt que comme des causes secondaires.
Ce sont l’hypothyroïdie, l’hypercorticisme et la tumeur hypothalamo-hypophysaire (cranio
pharyngiome).
Elles s’accompagnent le plus souvent de signes cliniques spécifiques (goitre pour l’hypothyroïdie, par exemple) et d’un ralentissement de la vitesse de croissance staturale, alors que celle-ci est souvent accélérée en cas d’obésité commune.
L’absence de ralentissement de la courbe staturale élimine une cause endocrinienne et rend inu-tile la réalisation d’explorations hormonales (TSH, cortisol libre urinaire, IGF-1).
On notera que la TSH est parfois augmentée, sans dysthyroïdie, chez les enfants présentant une obésité commune (10 à 20 %).
Obésité dite commune : cause principale d’obésité de l’enfant.
Retard mental, dysmorphie, hyperphagie intense, ± retard statural, hypogonadisme → évoquer une cause syndromique.
Obésité précoce et sévère, hyperphagie intense → évoquer une cause monogénique connue.
Absence de ralentissement de la vitesse staturale → inutile de rechercher une cause endocrinienne.
C. Diagnostic des complications
1. Généralités
La recherche clinique de complications doit toujours être assurée, bien que les complications somatiques sévères soient rares en pédiatrie, contrairement à l’obésité de l’adulte.
2. Points forts sur les principales complications (tableau 16.2)
Complications métaboliques et nutritionnelles
L’insulinorésistance concerne plus de la moitié des enfants obèses. Elle est traduite par une hyperinsulinémie. Elle est parfois responsable d’un acanthosis nigricans (pigmentation noirâtre reposant sur une peau rugueuse, épaissie et quadrillée, localisée principalement aux aisselles, au cou et aux régions génitocrurales).
L’intolérance au glucose concerne 5 à 10 % des enfants obèses. Elle est définie par une glycémie à jeun normale et une glycémie > 7,8 mmol/l et < 11,1 mmol/l, 120 minutes après ingestion du glucose au cours d’une HGPO. En pratique clinique, la réalisation d’une HGPO n’est pas utile car ni l’insulinorésistance ni l’intolérance au glucose ne requièrent de traitement spécifique de manière consensuelle.
Le diabète est rare en France chez l’enfant obèse, sauf dans les populations d’origine africaine. En pratique clinique, le dosage de la glycémie à jeun à la recherche d’un diabète doit être réservé à l’enfant de plus de 10 ans dans des cas particuliers (obésité sévère, antécédents familiaux de diabète précoce chez un enfant à peau noire ou métissée, suspicion clinique de diabète).
Une dyslipidémie atteint environ 20 % des enfants obèses. Elle inclut principalement une diminution du HDL-cholestérol et une hypertriglycéridémie, plus rarement une élévation du LDL-cholestérol.
Elle ne nécessite presque toujours aucune prise en charge spécifique, en dehors de celle de l’obésité.
La recherche systématique d’une dyslipidémie doit être limitée aux enfants ayant des antécédents familiaux d’hypercholestérolémie, à la recherche d’une hypercholestérolémie familiale, seule dyslipidémie nécessitant une prise en charge thérapeutique chez l’enfant obèse.
La carence en vitamine D est plus fréquente, justifiant de doubler la supplémentation chez les enfants obèses. Elle est due à un piégeage dans le tissu adipeux (vitamine liposoluble) et/ou à une diminution de la protéine porteuse (DBP).
La carence en fer est également plus fréquente en raison d’une augmentation de la sécrétion d’hepcidine, une molécule inhibant l’absorption intestinale du fer. Une consommation carnée suffisante doit être assurée et une supplémentation prescrite en cas de carence avérée.
Complications endocriniennes
Une accélération de la croissance staturale est le plus souvent observée dans l’obésité commune, avec une taille définitive normale.
La puberté débute parfois plus tôt chez les filles obèses (entre 8 et 10 ans), mais elle survient le plus souvent à un âge normal chez les garçons.
Les garçons se plaignent parfois de verge enfouie dans la masse graisseuse hypogastrique ou d’adipogynécomastie (accumulation de graisse au niveau de la région mammaire simulant le développement de seins). Ces dysmorphies peuvent induire de sérieux troubles psychologiques.
Il existe parfois des troubles des règles (spanioménorrhée ou aménorrhée) chez les adolescentes. Le syndrome des ovaires polykystiques, se manifestant entre autres par une hyperandrogénie, est plus rare que chez l’adulte.
Complications respiratoires et cardiovasculaires
L’asthme atteint avec une plus grande fréquence les enfants obèses. Il s’exprime souvent par une dyspnée ou une toux à l’effort. Son traitement est indispensable pour améliorer la tolérance de l’effort physique.
Le syndrome d’apnées obstructives du sommeil (SAOS) est rare mais potentiellement grave. At-teignant principalement les enfants souffrant d’obésité sévère, il se manifeste par des ronflements nocturnes importants avec reprise inspiratoire bruyante, une somnolence diurne ou des troubles du sommeil, parfois une nycturie ou une énurésie. En plus de la réduction pondérale, le SAOS nécessite la mise en route d’une pression positive continue nasale dans les formes sévères (voir chapitre 62).
Les pressions artérielles systolique et diastolique de repos sont souvent augmentées, mais elles dépassent rarement les limites physiologiques. L’hypertension artérielle (voir chapitre 50) atteint moins de 5 % des enfants obèses.
Complications digestives
Une stéatose hépatique est rencontrée chez 10 à 20 % des enfants obèses et pas uniquement dans les surcharges pondérales sévères.
Elle s’exprime principalement par une augmentation modérée des transaminases à 1,5 à 2 fois la normale ; une élévation plus importante ou persistante de celles-ci ou une augmentation des γGT doivent faire évoquer une stéatohépatite ou une autre hépatopathie. Son évolution est presque toujours bénigne chez l’enfant.
Elle n’est recherchée qu’en cas d’antécédents familiaux de maladie hépatique (notamment de stéatohépatite) ou dans les obésités sévères.
Complications orthopédiques
Le genu valgum est fréquent. Il ne se complique ni de douleurs ni d’arthrose.
Des douleurs musculaires et articulaires des membres inférieurs ou du dos sont fréquentes et parfois invalidantes, mais elles ne traduisent pas l’existence d’anomalies articulaires dégénératives (comme c’est le cas chez l’adulte).
L’épiphysiolyse de la tête fémorale est beaucoup plus rare mais constitue une urgence orthopédique. Sous l’effet du poids et surtout de facteurs dysmétaboliques, une dysplasie du cartilage de conjugaison apparaît, entraînant une diminution de sa résistance mécanique puis un glissement de la tête fémorale sur la métaphyse. Elle se manifeste par des douleurs de hanche ou du genou d’installation progressive (voir chapitre 70).
Complications psychosociales
Quel que soit l’âge, l’obésité entraîne une souffrance psychologique de l’enfant dont l’expression clinique est très variée.
Une souffrance vis-à-vis du regard d’autrui, mais aussi liée à sa propre image du corps chez les plus âgés, est quasi-systématique dès que l’enfant est susceptible d’en prendre conscience. Elle peut être à l’origine d’une déscolarisation et peut dans certains cas aggraver l’obésité.
La discrimination sociale de l’enfant obèse existe également dès le plus jeune âge, notamment en milieu scolaire.
Tableau 16.2. ![]() Complications dans le cadre d’une obésité commune de l’enfant.
Complications dans le cadre d’une obésité commune de l’enfant.
| Complications métaboliques et endocriniennes |
|
| Complications nutritionnelles |
|
| Complications cardiovasculaires et respiratoires |
|
| Complications orthopédiques |
|
| Complications digestives |
|
| Complications morphologiques et cutanées |
|
| Complications psychosociales |
|
3. Indications d’une enquête paraclinique
Aucun bilan paraclinique systématique à la recherche de complications n’est habituellement nécessaire. La prescription d’examens complémentaires doit être guidée par les données de l’interrogatoire et de l’examen clinique.
Les recommandations de la HAS de 2022 sont plus larges que celles proposées par la plupart des experts. Si elles ne préconisent pas de bilan systématique chez l’enfant ayant un surpoids, elles suggèrent chez l’enfant obèse la recherche d’une dyslipidémie en cas d’antécédents familiaux d’hypercholestérolémie, la recherche d’un diabète en cas d’antécédents familiaux de diabète de type 2 au premier ou deuxième degré, et la réalisation d’un bilan hépatique.
Recherche des complications : clinique avant tout.
Complications somatiques graves : très rares chez l’enfant obèse, contrairement à l’adulte obèse.
III. Argumenter l’attitude thérapeutique et planifier le suivi
A. Modalités de prise en charge thérapeutique
La prise en charge de l’enfant obèse doit avoir comme objectifs :
- négativation de la balance énergétique, avec deux critères d’efficacité croissante sur l’excès pondéral (estimé par l’IMC en déviation standard [DS] car l’IMC en valeur absolue augmente physiologiquement à partir de l’âge de 6 ans) : stabilisation ou réduction de l’IMC (DS) ;
- modification durable des comportements vis-à-vis de l’alimentation : dans la mesure où les in-gesta énergétiques spontanés sont augmentés par rapport aux besoins pour l’âge et le sexe, la restriction volontaire des apports énergétiques est un moyen thérapeutique incontournable.
Cette prise en charge doit être multidisciplinaire et individualisée (tableau 16.3).
Tableau 16.3. ![]() Prise en charge thérapeutique de l’enfant obèse.
Prise en charge thérapeutique de l’enfant obèse.
| Prise en charge diététique Accompagner vers : |
|
| Mettre en place une activité physique régulière et lutter contre la sédentarité |
|
| Éducation thérapeutique, soutien psychologique |
|
Il est très difficile de traiter l’obésité si l’enfant et sa famille ne sont pas motivés.
Des inhibiteurs de l’appétit sont en cours d’évaluation chez l’adolescent. Pour l’instant, seul le liraglutide (injections SC) a l’AMM pour être prescrit chez l’adolescent après l’âge de 12 ans. Son efficacité est variable selon les individus. Il n’est pas remboursé par l’Assurance maladie.
La chirurgie bariatrique peut être proposée en cas d’obésité sévère (IMC > 40 kg/m2) ou compliquée (IMC > 35 kg/m2 + une des comorbidités suivantes : diabète, apnées du sommeil, stéatohépatite, hypertension intracrânienne) chez l’adolescent après 15 ans. Elle est réservée à des centres spécialisés et sera sans doute de moins en moins pratiquée du fait de la possibilité d’utiliser des thérapeutiques innovantes.
B. Suivi et pronostic
Le suivi de l’enfant et de sa famille est multidisciplinaire.
Il s’inscrit dans la durée, grâce à un partenariat établi entre l’enfant et sa famille, le médecin traitant, le diététicien et le spécialiste référent.
L’enfant est suivi en consultation selon un rythme à adapter en fonction de l’évolution pondérale et de la motivation de l’enfant et de sa famille.
Pour la majorité des enfants pris en charge, une stabilisation voire une réduction de l’excès pondéral est obtenue à moyen terme. Mais près des deux tiers des enfants obèses d’âge scolaire (notamment ceux qui le sont à l’adolescence) seront encore en surcharge pondérale à l’âge adulte.
Le bas niveau socio-économique est le principal facteur de persistance de l’excès pondéral à l’âge adulte.
Prise en charge multidisciplinaire : réduction des apports énergétiques, augmentation de l’activité physique, soutien psychologique.
Le risque de rester en surcharge pondérale à l’âge adulte est élevé, en particulier à l’adolescence.
IV. Mesures de prévention
A. Prévention primaire
Compte tenu de l’efficacité non démontrée des mesures préventives primaires (éducation nutritionnelle à l’école, messages sanitaires divers), il faut se garder des attitudes excessives, du fait de potentiels effets délétères (induction de troubles du comportement alimentaire, stigmatisation des enfants et adolescents obèses).
B. Prévention secondaire
Les deux signes prédictifs d’obésité ultérieure sont :
- la précocité du rebond d’adiposité : avant l’âge de 6 ans ;
- l’obésité chez au moins l’un des parents.
L’efficacité de la prise en charge d’un enfant en cas de rebond précoce de l’adiposité n’a cependant pas fait la preuve de son efficacité.
Références

|
HAS. Surpoids et obésité de l’enfant et de l’adolescent. Guide du parcours de soin. 2022. https://www.has-sante.fr/upload/docs/application/pdf/2022-02/guide_parcours_surpoids_et_obesite_enfants_adolescents.pdf |

|
HAS. Critères d’éligibilité pour la réalisation d’une chirurgie bariatrique chez les moins de 18 ans. Fiche mémo. 2016. http://www.has-sante.fr/portail/upload/docs/application/pdf/2016-03/fm_chirurgie_bariatrique__v3_2.pdf |
