Objectifs pédagogiques
- Diagnostiquer les troubles du sommeil du nourrisson, de l’enfant et de l’adulte.
- Connaître les principes de la prise en charge.
Avant de commencer…
Troubles du sommeil de l’enfant
Les troubles du sommeil les plus fréquents sont les insomnies, définies par un trouble de l’initiation ou du main-tien du sommeil, généralement secondaires à des difficultés éducatives au sein de la famille.
Ce chapitre traite particulièrement du syndrome d’apnées-hypopnées obstructives du sommeil (SAHOS).
SAHOS de l’enfant
La principale cause est l’hypertrophie amygdalienne et/ou adénoïdienne.
Les signes cliniques associés regroupent des symptômes nocturnes et diurnes qui sont très variables d’un enfant à l’autre et qui sont peu corrélés aux résultats de l’examen du sommeil.
La polysomnographie est l’examen de référence pour poser le diagnostic et pour apprécier la sévérité du SAHOS, mais sa réalisation n’est pas systématique. Elle est inutile lorsque l’hypertrophie amygdalienne est évidente chez un enfant âgé de plus de 3 ans, par ailleurs bien portant.
L’adénoïdo-amygdalectomie est le traitement de première intention. Son efficacité est moindre en cas d’obésité ou lors d’une pathologie malformative cranio-maxillo-faciale associée.
I. Pour bien comprendre
A. Sommeil normal
1. Spécificités pédiatriques
Un enfant dort plus qu’un adulte et à des moments différents (tableau 62.1).
La durée normale du sommeil diminue avec l’âge ; la sieste de l’après-midi disparaît vers l’âge de 3 à 5 ans.
L’architecture du sommeil évolue en fonction de l’âge : le pourcentage de sommeil paradoxal (ou agité) diminue pendant la première année pour se stabiliser ensuite, tout comme le sommeil léger.
Tableau 62.1. ![]() Quantité normale de sommeil en fonction de l’âge.
Quantité normale de sommeil en fonction de l’âge.
| Âge | Durée idéale de sommeil |
|---|---|
| 0–2 mois | 10–19 h |
| 2–12 mois | 9–10 h (nuit) + 3–4 h (siestes) |
| 1–3 ans | 9,5–10,5 h (nuit) + 2–3 h (siestes) |
| 3–6 ans | 9–10 h |
| 6–12 ans | 9–10 h |
| 13–18 ans | Besoins : 9–9,5 h ; durée réelle : 7–7,5 h |
2. Modifications physiologiques de la respiration au cours du sommeil
La respiration étant moins efficace pendant le sommeil, on observe une augmentation physiologique d’environ 5 à 10 mmHg de la pression partielle en CO2 et une diminution d’environ 2 à 3 % de l’oxymétrie de pouls (SpO2) pendant le sommeil chez le sujet sain.
3. Quelques règles d’hygiène du sommeil
Conseils pouvant être donnés aux familles :
- régularité des horaires de coucher, de lever, de sieste et de repas ;
- sortir dans la journée et s’exposer à la lumière du jour ;
- faire des activités physiques dans la journée, avant 18 heures ;
- limiter au maximum tous les objets connectés, surtout en fin de journée ;
- la chambre à coucher doit être confortable, calme, propre, bien aérée avant le coucher avec une température optimale autour de 18 °C ;
- le lit ne doit servir qu’à dormir et ne doit pas servir à manger ou travailler ;
- une activité rituelle le soir avant de se coucher favorise l’endormissement ;
- le dîner doit être léger mais consistant : il doit privilégier les sucres lents, éviter les protéines et les aliments trop gras ; il faut éviter les aliments excitants après 14 heures (café, thé, cola).
B. Troubles du sommeil : généralités
1. Définitions
Un trouble du sommeil est un phénomène perturbant le cycle du sommeil et susceptible d’entraîner des conséquences chez l’enfant.
Les dysomnies correspondent à la perturbation de la quantité, de la qualité ou des horaires du sommeil.
On y classe les insomnies et troubles du rythme circadien ainsi que les hypersomnies.
Les parasomnies correspondent aux phénomènes anormaux survenant lors du sommeil.
On y classe par exemple les cauchemars, les terreurs nocturnes et le somnambulisme.
2. Quand y penser chez un enfant ?
- Difficultés à l’endormissement ou au maintien du sommeil, pleurs nocturnes.
- Réveil difficile, réapparition ou persistance de siestes après l’âge de 6 ans.
- Endormissement en classe, agitation ou irritabilité, troubles de l’humeur.
C. Troubles du sommeil : étiologie
1. Dyssomnies
Insomnies
Les insomnies du nourrisson et du jeune enfant peuvent traduire des difficultés éducatives : conditionnement anormal à l’endormissement, prise alimentaire nocturne, insuffisance de limites. Certains troubles correspondent à des comportements non pathologiques : la peur du noir et le désir de dormir avec les parents sont habituels chez le jeune enfant et transitoires.
Parfois, des causes médicales peuvent expliquer ces insomnies. Certaines sont bénignes : coliques du nourrisson, erreurs alimentaires. D’autres nécessitent d’être diagnostiquées : rhinite et asthme, diabète (énurésie secondaire), maladie neurologique (rarement).
Certains enfants ont une insomnie idiopathique durable. Ce type d’insomnie pédiatrique a des liens avec le déficit d’attention-hyperactivité ou des troubles du comportement.
Les insomnies du grand enfant et de l’adolescent correspondent généralement à un syndrome de retard de phase. Ce trouble du sommeil est la conséquence d’un coucher et d’un lever trop tardifs. Il est conditionné par des facteurs environnementaux et sociaux (activités scolaires et parascolaires, pression scolaire, utilisation excessive des tablettes, ordinateurs, portables, diminution de la surveillance parentale).
Il convient de dépister également à ces âges des symptômes de dépression car l’insomnie peut en être un symptôme révélateur.
Le diagnostic différentiel d’une insomnie chronique est l’enfant « petit dormeur » ; il existe naturellement des sujets « courts » et « grands » dormeurs.
À rechercher devant une insomnie chronique :
- une privation du sommeil ;
- des causes favorisantes : traumatisme psychologique, événement familial ;
- déficit d’attention-hyperactivité ;
- une étiologie organique.
La prise en charge repose sur des principes d’hygiène de sommeil (voir supra) et un abord comportemental ; la prescription de médicaments doit rester exceptionnelle.
Hypersomnies
L’hypersomnie idiopathique survient après l’âge de 10 ans. Elle se caractérise par une somnolence diurne excessive sans attaque de sommeil ni accès de cataplexie, sans hallucinations hypnagogiques (hallucinations visuelles et auditives à l’endormissement) ni paralysie du sommeil.
Ces caractéristiques sont en revanche présentes au cours de la narcolepsie, survenant chez des enfants habituellement plus âgés.
Les causes principales d’hypersomnie sont le syndrome d’insuffisance du sommeil induit par le comportement, l’hypersomnie non due à la prise d’une substance ou d’une maladie (hypersomnie non organique), beaucoup plus rarement les hypersomnies d’origine centrale (narcolepsie, hypersomnie idiopathique) et, enfin, les hypersomnies liées à des causes médicales, chirurgicales, post-traumatiques ou liées à la prise d’une substance, alcool ou drogue.
L’interrogatoire recherche un temps de sommeil ou passé au lit > 3 heures par rapport au temps moyen pour l’âge, la persistance ou la réapparition de siestes, l’apparition de troubles comportementaux ou émotionnels, un sommeil anormalement agité avec terreurs ou somnambulisme. L’échelle d’Epworth adaptée à la pédiatrie permet de quantifier la somnolence subjective (score anormal si > 15).
La polysomnographie élimine une pathologie associée comme le SAHOS. Des tests itératifs de latence d’endomissement (TILE) permettent de confirmer le diagnostic d’une hypersomnie. La présence de deux endormissements en sommeil paradoxal (REM) caractérise la narcolepsie.
Le diagnostic différentiel principal de ces hypersomnies est le SAHOS (justifiant donc la réalisation d’une polysomnographie).
2. Parasomnies
Les cauchemars surviennent chez l’enfant âgé de 3 à 6 ans, durant le sommeil paradoxal. L’enfant est réveillé par des rêves angoissants. Il n’y a pas d’amnésie au décours.
Les terreurs nocturnes surviennent chez l’enfant prépubère, avec un réveil brutal quelques heures après l’endormissement. L’enfant est retrouvé en train de crier, avec une peur intense non apaisée par les parents. Il a une amnésie totale de l’épisode le lendemain matin.
Le somnambulisme survient le plus souvent chez le garçon âgé de 7 à 12 ans, au cours de la première moitié de nuit. L’enfant se lève et déambule, a parfois une activité plus complexe, puis se recouche. Il a une amnésie totale de l’épisode le lendemain matin.
Il convient également d’évoquer dans ce contexte l’éventualité d’un autre diagnostic : une épilepsie focale (frontale, temporale) ou une prise de toxiques en cas de présentation atypique ou de survenue durant l’éveil.
Le syndrome des jambes sans repos (SJSR) est un trouble sensorimoteur caractérisé par une urgence irrésistible à bouger les jambes, accompagné par des sensations d’inconfort des jambes qui sont soulagées par le mouvement et sont accentuées le soir ou la nuit au repos. Le déficit en fer est impliqué dans la physiopathologie du SJSR, nécessitant le dosage systématique de la ferritine et un traitement substitutif en cas de carence en fer.
Insomnies : difficultés éducatives familiales chez le nourrisson et le jeune enfant, syndrome de retard de phase chez le grand enfant et l’adolescent.
Parasomnies : cauchemars, terreurs nocturnes, somnambulisme.
Ne pas méconnaître une cause organique.
II. Syndrome d’apnées-hypopnées obstructives du sommeil
A. Généralités
1. Définition
Le syndrome d’apnées-hypopnées obstructives du sommeil (SAHOS) de l’enfant est caractérisé par des épisodes répétés de fermeture complète des voies aériennes supérieures (apnée : diminution ≥ 90 % du débit respiratoire) ou partielle (hypopnée : diminution ≥ 30 % du débit respiratoire) pendant le sommeil.
Le SAHOS est défini par un index d’apnées-hypopnées obstructives (IAOH) ≥ 1,5 événements/heure de sommeil.
Sa sévérité est évaluée sur la valeur de l’IAOH :
- IAOH < 1,5/heure : absence de SAHOS ;
- 1,5 ≤ IAOH < 5/heure : SAHOS léger ;
- 5 ≤ IAOH < 10/heure : SAHOS modéré ;
- IAOH ≥ 10/heure : SAHOS sévère.
2. Épidémiologie
Le SAHOS touche 1 à 4 % des enfants, avec un pic de fréquence entre les âges de 3 à 6 ans du fait de l’hypertrophie des végétations adénoïdes et des amygdales dans un petit massif facial.
3. Facteurs de risque
Un terrain à risque doit être systématiquement recherché : obésité, allergie, anomalie orthodontique.
L’enfant ayant une malformation ou une déformation maxillofaciale ou des voies aériennes supérieures rétrécissant les voies aériennes est plus à risque de SAHOS (cranio-facio-sténose, achondroplasie, hypoplasie ou microsomie faciale, syndrome de Pierre Robin, mucopolysaccharidose, trisomie 21, syndrome de Prader-Willi), ce qui en justifie la recherche systématique.
4. Conséquences du SAHOS
La morbidité neurocognitive est la conséquence la plus fréquente et la plus sévère du SAHOS. Elle se traduit par une hyperactivité, une irritabilité, voire un déficit d’attention-hyperactivité (TDAH). L’agitation, un défaut de concentration ou de mémoire sont souvent au premier plan et peuvent être responsables de difficultés ou d’un retard scolaire. En effet, les épisodes répétés d’apnées ou d’hypopnées sont responsables de réveils et microréveils, entraînant une fragmentation et une mauvaise qualité du sommeil. Une amélioration des troubles neurocognitifs est observée après traitement du SAHOS dans la très grande majorité des cas.
La morbidité cardiovasculaire est moins importante que chez l’adulte. Les épisodes répétés d’obstruction des voies aériennes sont associés à une hyperactivation sympathique avec augmentation de la fréquence cardiaque et de la tension artérielle.
La morbidité métabolique consiste en une dysrégulation du système glucidique et lipidique.
Ces perturbations sont très variables d’un enfant à l’autre. Une susceptibilité spécifique liée à l’âge, au terrain, à la durée et l’importance du SAHOS, peut expliquer ces différences.
B. Diagnostic
1. Enquête clinique
Symptômes cliniques
Le SAHOS est associé à des symptômes cliniques nocturnes et diurnes dont la présence et la sévérité sont variables (tableau 62.2).
Aucun symptôme n’est spécifique ou pathognomonique du SAHOS et aucune association de signes, même si on y intègre l’examen physique, n’est suffisamment informative pour poser ou infirmer le diagnostic de SAHOS chez l’enfant.
Il est important de réaliser un recueil d’informations le plus complet possible afin de contrôler au mieux les modifications cliniques observées sous traitement.
Tableau 62.2. ![]() Symptômes évocateurs d’un SAHOS.
Symptômes évocateurs d’un SAHOS.
| Symptômes nocturnes | Symptômes diurnes | Signes ORL et dento-faciaux | |
|---|---|---|---|
| Critères majeurs |
|
|
|
| Critères mineurs |
|
|
|
Source : Aubertin G, Schroder C, Sevin F, et al. Diagnostic clinique du syndrome d’apnees obstructives du sommeil de l’enfant : diagnostic clinique. Arch Pediatr 2017;24(Suppl):S7-S15.
Examen physique
Il est indispensable mais est insuffisant pour poser le diagnostic de SAHOS.
Il s’accompagne de la réalisation d’une nasofibroscopie.
Cet examen doit être fait par un médecin ORL qui analyse les fosses nasales à la recherche d’une hypertrophie adénoïdienne, le pharynx à la recherche d’une hypertrophie amygdalienne (fig. 62.2), et d’éventuelles anomalies ou malformations associées des voies aériennes supérieures. L’examen recherche une malposition dentaire ou une anomalie maxillo-faciale.
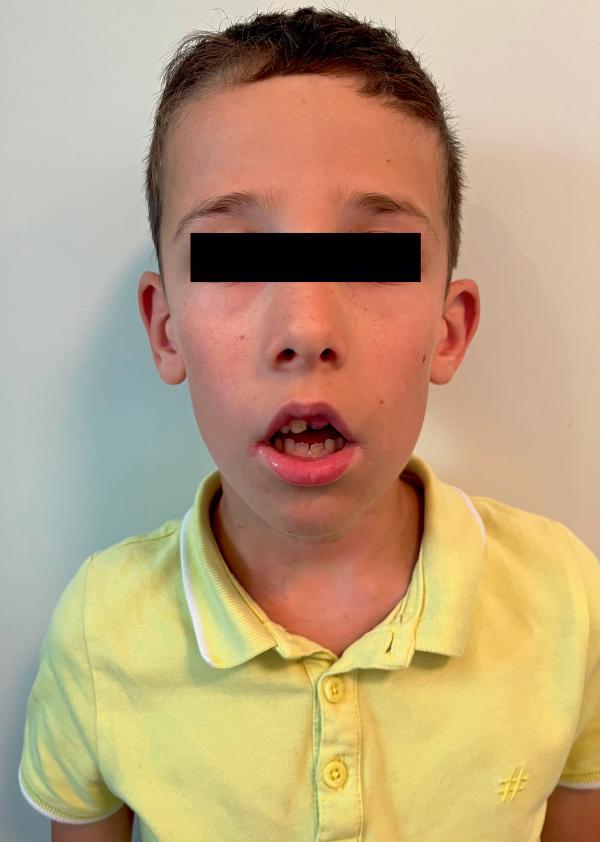
Fig. 62.1. ![]() Faciès adénoïdien.
Faciès adénoïdien.
Déficit de croissance transversale, cernes, béance antérieure, langue basse.
Source : Pierre-Jean Monteyrol.
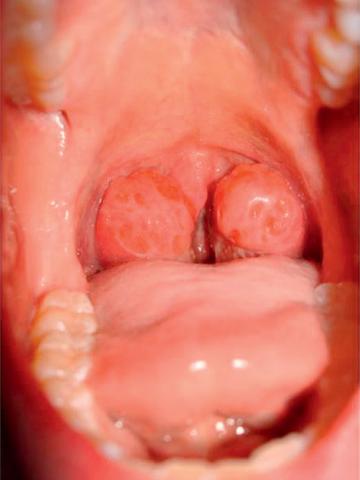
Fig. 62.2. ![]() Hypertrophie amygdalienne.
Hypertrophie amygdalienne.
Réimprimé à partir de : Aubertin G, Schröder C, Sevin F, Clouteau F, Lamblin M-D, Vecchierini M-F. Diagnostic clinique du syndrome d’apnées obstructives du sommeil de l’enfant. Arch Pediatr 2017;24(Suppl. 1):S7–S15.
2. Enquête paraclinique
Polysomnographie
La polysomnographie en milieu hospitalier est l’examen de référence pour le diagnostic des SAHOS de l’enfant.
Elle est également indiquée pour le dépistage d’un SAHOS dans certaines pathologies de la tête et du cou (malformations) et maladies génétiques entraînant des anomalies des voies aériennes supérieures (par exemple, trisomie 21).
Cet examen se déroule la nuit dans une chambre-laboratoire d’un centre des troubles du sommeil. La polysomnographie peut éventuellement être réalisée à domicile ou pendant une sieste dans la journée chez le jeune nourrisson.
Elle est définie par la HAS comme comportant l’enregistrement des six signaux de quantification des stades du sommeil (au minimum trois EEG, deux EOG, un EMG mentonnier), auxquels sont ajoutés les signaux de la respiration et des échanges gazeux : débit aérien naso-buccal avec le ronflement, mouvements thoraco-abdominaux, position, actigraphie, oxymétrie de pouls et gaz carbonique transcutané.
Elle se justifie lors d’un SAHOS potentiellement lié à une hypertrophie amygdalienne lorsque :
- l’amygdalectomie risque de ne pas être suffisante pour corriger le trouble obstructif du sommeil : existence d’une pathologie associée (obésité morbide, anomalie craniofaciale ou des voies aériennes supérieures, maladie neuromusculaire) ;
- il y a discordance entre l’examen clinique et les troubles respiratoires : obstacle amygdalien ou adénoïdien cliniquement modeste ;
- il existe un risque opératoire élevé : troubles de l’hémostase, hypertension artérielle.
Il n’y a pas de corrélation entre le volume des amygdales noté à l’examen, l’importance des signes cliniques, et les résultats de la polysomnographie.
En l’absence d’accès simple à une polysomnographie, la réalisation d’une polygraphie respiratoire est possible lorsqu’elle est réalisée et interprétée par une équipe spécialisée.
Elle est définie par la HAS comme comportant au minimum cinq signaux enregistrés, dont le débit aérien naso-buccal, les mouvements respiratoires thoraco-abdominaux, l’oxymétrie, la fréquence cardiaque ou l’ECG, et la position corporelle.
Examens radiologiques
Aucun examen radiologique n’a sa place dans la prise en charge de première intention d’un enfant suspect de troubles respiratoires du sommeil.
La nasofibroscopie, indispensable à l’évaluation clinique, permet de se passer de la radiographie de cavum, qui ne doit plus être réalisée. L’examen tomodensitométrique n’a pas d’indication dans le SAHOS typique de l’enfant.
C. Prise en charge
1. Adénoïdo-amygdalectomie
L’adénoïdo-amygdalectomie est le traitement de première intention du SAHOS en cas d’hypertrophie modérée à importante des tissus lymphoïdes.
2. Traitement anti-inflammatoire
L’association d’un corticoïde nasal et d’un antileucotriène pendant 3 mois a montré dans certains cas son efficacité. Des antihistaminiques peuvent être utilisés, même en l’absence d’allergie.
Aucun médicament n’a d’AMM en France dans cette indication.
3. Particularités thérapeutiques chez l’enfant avec comorbidités
Une prise en charge multidisciplinaire spécialisée est indispensable pour limiter l’impact de la comorbidité (par exemple, prise en charge de l’obésité de l’enfant).
La pression positive continue (PPC) est le traitement de choix du SAHOS sévère persistant après la chirurgie ORL. Elle consiste en la délivrance d’une pression positive pendant tout le cycle respiratoire par un masque nasal, facial ou par des canules nasales en fonction de l’âge, de la tolérance, et de la morphologie faciale. Sa mise en route relève d’un centre spécialisé.
Un traitement orthodontique est indiqué lorsqu’il existe une malposition dentaire ou une anomalie orthodontique. Selon les cas, il est réalisé soit isolément, soit associé à une adénoïdo-amygdalectomie.
La neurochirurgie, ou la chirurgie maxillo-faciale sont réservées à des cas bien particuliers.
SAHOS de l’enfant jeune sans comorbidité sévère
- Prévalence : 1–4 %.
- Âge : 3–6 ans.
- Physiopathologie : hypertrophie (isolée) des amygdales ± végétations adénoïdes.
- Sévérité : variable.
- Évolution : amélioration spontanée dans 30–50 % cas.
- Facteurs de risque : obésité ; allergie respiratoire, prématurité, asthme.
- Diagnostic : interrogatoire et examen clinique ; pas de polysomnographie.
- Conséquences : dysfonction neurocognitive ; stress cardiovasculaire ; syndrome métabolique.
- Traitement : adénoïdo-amygdalectomie.
Références
Aubertin G, et al. Management of obstructive sleep-disordered breathing type 1 in children and adolescent – A french consensus. Arch Pediatr 2023;30(7):510-6.
