Objectifs pédagogiques
- Connaître l’épidémiologie des méningites et encéphalites chez l’adulte et l’enfant.
- Diagnostiquer un purpura fulminans (voir item 332), une méningite, une ménin-go-
encéphalite. - Connaître les principaux agents infectieux responsables de méningites, de mé-ningo-encéphalite, d’abcès cérébraux.
- Connaître la conduite à tenir dont le traitement en urgence face à un purpura fulminans, une suspicion de méningite ou de méningo-encéphalite, au domicile, au cabinet médical et aux urgences hospitalières.
- Hiérarchiser les examens complémentaires en cas de suspicion de méningite, de méningo-encéphalite.
- Interpréter le résultat d’un examen du liquide céphalorachidien.
- Connaître le traitement de première intention d’une méningite communautaire présumée bactérienne.
- Connaître les recommandations de la prophylaxie des infections à méningo-coque dans l’entourage d’un cas de méningite à méningocoque.
Avant de commencer…
Le diagnostic d’infection neuroméningée doit être systématiquement :
- suspecté rapidement sur les données cliniques (plus difficilement évaluables chez le nourrisson) ;
- évalué en termes de gravité (états hémodynamique et neurologique) ;
- confirmé par l’étude du liquide cérébrospinal (LCS) obtenu par ponction lombaire.
La prise en charge thérapeutique initiale des méningites bactériennes repose sur :
- une antibiothérapie IV la plus précoce possible, probabiliste et active sur :
- le pneumocoque (S. pneumoniae) : chez le nourrisson (première bactérie avant 1 an) ;
- le méningocoque (N. meningitidis) : à tout âge ;
- avec comme objectif premier la stérilisation rapide du LCS.
Le suivi des formes bactériennes nécessite des évaluations neurologiques, cognitives et auditives.
Des mesures préventives pour les sujets contacts sont indiquées pour les méningites à méningocoque.
Ce qui distingue les méningites purulentes de l’enfant de celles de l’adulte :
- une sémiologie clinique spécifique chez le nourrisson (hypotonie, geignements, fièvre isolée…) ;
- la moindre fréquence des tableaux neurologiques aigus, tels que signes neurologiques de localisation, crises épileptiques, ne justifiant que rarement une imagerie cérébrale ;
- la nécessité d’un suivi d’au moins 1 an pour le dépistage d’une surdité sévère susceptible de bénéficier précocement de nouvelles techniques d’implants cochléaires.
Méningites
I. Pour bien comprendre
A. Épidémiologie
1. Méningites virales, méningites infectieuses non purulentes
Les méningites virales sont les plus fréquentes des méningites infectieuses chez l’enfant.
Le diagnostic est suspecté devant l’identification d’un LCS d’aspect optique non purulent (translucide, parfois opalescent) avec une réaction cellulaire modérée (habituellement < 500 éléments/mm3), de formule lymphocytaire ou panachée (50–100 % de lymphocytes), demeurant stérile à la culture.
Virus les plus souvent retrouvés :
- entérovirus dont Echovirus (surtout) ;
- entérovirus de type coxsackie virus (plus rare) ;
- mais aussi : HHV6, virus de la varicelle et du zona, virus EBV ou virus ourlien ;
- en redoutant toujours : HSV (atteinte encéphalique sévère).
Toutes les méningites non purulentes ne sont pas d’origine virale.
Des bactéries sont plus rarement en cause : BK (enfants immigrés ou immunodéprimés) et Listeria (exceptionnelle).
2. Méningites bactériennes, méningites à liquide purulent
L’incidence des méningites bactériennes est beaucoup plus élevée chez l’enfant que chez l’adulte. Elle est estimée tous âges et tous germes confondus à 2,2 cas pour 100 000 habitants en France et à 50 cas pour 100 000 habitants dans les pays en développement.
La mortalité et les séquelles sont très élevées dans les pays en développement. Elles demeurent élevées également dans les pays industrialisés. En France, les méningites à pneumocoque ont, malgré le recours à des stratégies antibiotiques adaptées, une mortalité évaluée à 10 % et des séquelles chiffrées à 30 % en moyenne.
Deux bactéries prédominent chez l’enfant (nouveau-nés exclus) :
- Streptococcus pneumoniae : plus fréquent entre les âges de 2 et 12 mois ;
- Neisseria meningitidis : plus fréquent après l’âge de 12 mois.
Pneumocoque (Streptococcus pneumoniae)
S. pneumoniae est un germe de portage oropharyngé du jeune enfant.
L’introduction du vaccin pneumococcique conjugué à 13 valences s’est traduite par une réduction du pourcentage des méningites purulentes liées aux sérotypes inclus dans ce vaccin ainsi que par une réduction de la résistance de ceux-ci aux pénicillines.
Les méningites à pneumocoque sont plus fréquentes entre 2 et 12 mois de vie. Elles représentent environ 60 % des méningites bactériennes à ces âges.
En pédiatrie, la sensibilité parfois intermédiaire de S. pneumoniae aux bêtalactamines impose d’effectuer une détermination des CMI, de l’amoxicilline mais aussi du céfotaxime ou de la ceftriaxone pour toutes les souches isolées.
Méningocoque (Neisseria meningitidis)
N. meningitidis est une bactérie de portage du rhinopharynx.
Le germe possède une capsule polyosidique déterminant son sérogroupe. Parmi les 12 sérogroupes, 4 prédominent en France au cours des infections invasives à méningocoque (IIM) : B, C, W et Y. Si le B prédomine, la fréquence des autres sérogroupes varie selon les années et selon l’impact des stratégies vaccinales. La vaccination méningococcique C polyosidique conjuguée a fortement réduit l’incidence des IIM, dont les méningites, en rapport avec le sérogroupe C en France. La vaccination protéique (Bexsero®) a été mise en place chez le nourrisson en 2022 ; de par sa nature protéique, elle couvre en partie les IIM de tous les sérogroupes (B 85 %, C 37 %, W 62 %, Y 100 %). Actuellement en France, les IIM sont principalement dues aux sérogroupes B, Y et W ; les sérogroupes A et X ne circulent pas ou peu.
Les méningites à méningocoque sont plus fréquentes après 12 mois de vie. Elles représentent alors environ 60 % des méningites bactériennes dans cette tranche d’âge.
Le méningocoque reste sensible aux bêtalactamines même si un quart des souches invasives en France présentent une diminution de sensibilité à la pénicilline G et à l’amoxicilline (2020). Cependant, toutes les souches restent sensibles aux C3G avec des CMI suffisamment basses.
De telles données justifient le maintien d’un traitement en première intention par une C3G injectable (céfotaxime ou ceftriaxone).
Celui-ci assurant l’éradication du portage de ce germe, il dispense en outre de prescrire chez l’enfant atteint un traitement complémentaire par la rifampicine.
Autres germes
L’incidence des autres bactéries est moindre.
Le streptocoque du groupe B est le premier germe responsable des méningites chez les nourrissons âgés de moins de 2 mois ; il est constamment sensible à l’amoxicilline.
Escherichia coli est le second germe à cet âge.
Haemophilus influenzae b est rarement responsable de méningites depuis la généralisation en France de la vaccination anti-Haemophilus influenzae b. Son incidence augmente toutefois de nouveau depuis 2018.
D’autres bactéries sont responsables de méningites dans des contextes particuliers : salmonelles (enfants drépanocytaires), staphylocoque à coagulase négative et bacilles à Gram négatif (infections nosocomiales), germe opportuniste (immunodéprimés).
Virus : agent infectieux le plus fréquent des méningites de l’enfant.
Redouter : pneumocoque surtout avant l’âge de 1 an, méningocoque à tout âge.
B. Physiopathologie
L’envahissement des bactéries s’effectue quasi exclusivement par voie hématogène vers les espaces méningés et le LCS, qui est dépourvu d’activité bactéricide naturelle (à la différence du sérum).
La réponse de l’hôte à l’infection est délétère par la production de cytokines in situ qui entraîne une inflammation méningée considérable, générant un œdème cérébral et une réduction des flux vasculaires cérébraux responsables d’ischémie et de séquelles.
II. Diagnostiquer une méningite et distinguer cause virale et cause bactérienne
Le diagnostic de méningite est urgent et doit être :
- suspecté rapidement sur les données cliniques (plus difficile chez le nourrisson) ;
- évalué en termes de gravité sur l’état hémodynamique et neurologique ;
- confirmé par l’étude du LCS obtenu par ponction lombaire.
A. Enquête clinique
1. Données cliniques
Chez le nourrisson
Points d’appel (parfois difficiles à identifier) :
- fièvre élevée (parfois isolée) ;
- signes d’infection potentiellement sévère :
- teint pâle ou gris, caractère geignard, somnolence ;
- cris et pleurs inhabituels à la mobilisation, hyperirritabilité, inconsolabilité ;
- refus alimentaire, vomissements ;
- convulsions même brèves et apparemment isolées.
Signes neurologiques à particulièrement rechercher :
- bombement de la fontanelle antérieure (identifié en position assise en dehors des cris) ;
- modification du tonus neurologique :
- hypotonie de la nuque remplaçant souvent la raideur chez le nourrisson ;
- ou raideur anormale à la mobilisation du rachis avec rejet de la tête en arrière ;
- signes neurologiques de localisation.
Ce qui oriente vers une méningite bactérienne :
- signes de gravité immédiate (défaillance hémodynamique, HTIC menaçante) ;
- dans un contexte de convulsion fébrile : âge < 6 mois, caractère prolongé de l’épisode, absence de récupération au décours : signe neurologique ou trouble de conscience persistant.
Chez le grand enfant
Tableau clinique souvent proche de celui décrit chez l’adulte :
- fièvre à début le plus souvent brutal ;
- parfois au décours d’une infection des VAS ou d’un syndrome grippal ;
- syndrome méningé avec :
- céphalées, cervicalgies, photophobie ;
- vomissements et/ou refus alimentaire.
Signes neurologiques à particulièrement rechercher :
- raideur de nuque (flexion de nuque douloureuse et limitée, alors que les mouvements de latéralité restent possibles) ;
- signe de Brudzinski (flexion involontaire des membres inférieurs à l’antéflexion provoquée de la tête, fig. 37.1) ;
- signe de Kernig (résistance douloureuse à l’extension de la jambe après flexion de la cuisse sur le bassin) ;
- signes neurologiques de localisation.
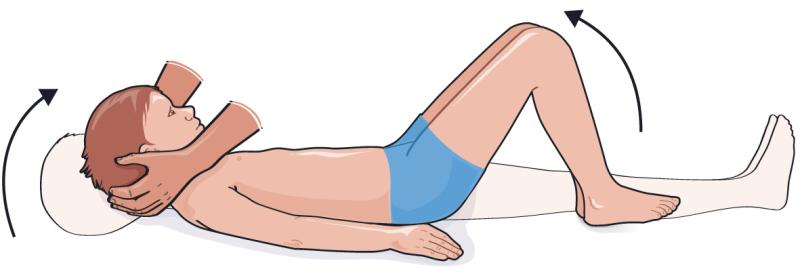
Fig. 37.1. ![]() Signe de Brudzinski.
Signe de Brudzinski.
Illustration de Carole Fumat.
2. Situations d’urgence à identifier
Signes de gravité hémodynamiques sepsis :
- signes : tachycardie, TRC ≥ 3 s, marbrures, extrémités froides, anurie ;
- urgence : remplissage vasculaire, contre-indication à la réalisation d’une PL.
Signes de gravité cutanés purpura fulminans (voir chapitre 24) :
- signes : choc hémodynamique avec purpura rapidement extensif et nécrotique (voir fig. 24.1) ;
- urgence : prise en charge hémodynamique, antibiothérapie par C3G IV/IM, transfert en réanimation.
Signes de gravité neurologiques HTIC, abcès ou empyème sous-dural :
- signes : troubles de conscience, coma, convulsions ;
- urgence : transfert en neurochirurgie, imagerie cérébrale préalable avant toute PL.
En cas de trouble de conscience fébrile, il faut savoir évoquer le diagnostic d’encéphalite herpétique (méningo-encéphalite), en raison de son pronostic redoutable.
Diagnostic de méningite à évoquer chez un nourrisson fébrile geignard et hypotonique.
Gravité = signes hémodynamiques, cutanés et neurologiques.
Toujours rechercher des signes d’atteinte encéphalitique.
B. Enquête paraclinique
1. Hiérarchiser les examens complémentaires
En pratique, deux examens biologiques sont recommandés :
- l’examen du LCS ;
- l’hémoculture.
Le diagnostic de méningite ne peut être affirmé que par l’examen du LCS qui doit être fait en urgence mais chez un patient stabilisé sur le plan hémodynamique, respiratoire et neurologique. La figure 37.2 et un lien vidéo en annexe illustrent le geste de ponction lombaire chez l’enfant.
La PL doit ainsi être différée en cas de :
- purpura fulminans et/ou instabilité hémodynamique urgence = remplissage vasculaire et injection de C3G ;
- signes évocateurs d’engagement cérébral urgence = hémoculture (si possible), injection de C3G et TDM cérébrale.
Le pronostic dépend essentiellement de la rapidité de mise en route de l’antibiothérapie IV.
Contre-indications à la PL en urgence en cas de suspicion de méningite bactérienne (d’après le consensus 2017) :
- instabilité hémodynamique ou respiratoire non contrôlée, a fortiori purpura fulminans ;
- anomalie de l’hémostase connue, traitement anticoagulant ou saignement actif évoquant une CIVD ;
- suspicion clinique de processus expansif intracrânien :
- déficit moteur : paralysie faciale centrale, paralysie oculomotrice, déficit du membre supérieur et/ou du membre inférieur ;
- crises épileptiques récentes et focales ;
- signes d’engagement cérébral :
- trouble de la vigilance ;
- et au moins un des symptômes suivants : anomalies pupillaires (mydriase fixée uni- ou bilatérale), dysautonomie (hypertension artérielle et bradycardie, anomalies du rythme ventilatoire), crises toniques postérieures, aréactivité aux stimulations, réactions de décortication ou de décérébration ;
- crises convulsives persistantes empêchant la réalisation de la PL.
L’imagerie cérébrale initiale préalable à la PL n’est indiquée qu’en cas de suspicion clinique de processus expansif intracrânien et/ou devant la présence de signes d’engagement cérébral.
Le fond d’œil, compte tenu des difficultés pratiques de sa réalisation en urgence ainsi que du retard d’apparition de l’œdème papillaire en cas d’œdème cérébral débutant, n’est pas utile avant la PL.
Contre-indication à la PL : purpura fulminans et/ou troubles hémodynamiques, signes d’engagement cérébral. Mesures thérapeutiques urgentes en priorité.
L’imagerie cérébrale, si indiquée, ne doit pas retarder l’antibiothérapie (à initier avant imagerie et PL).
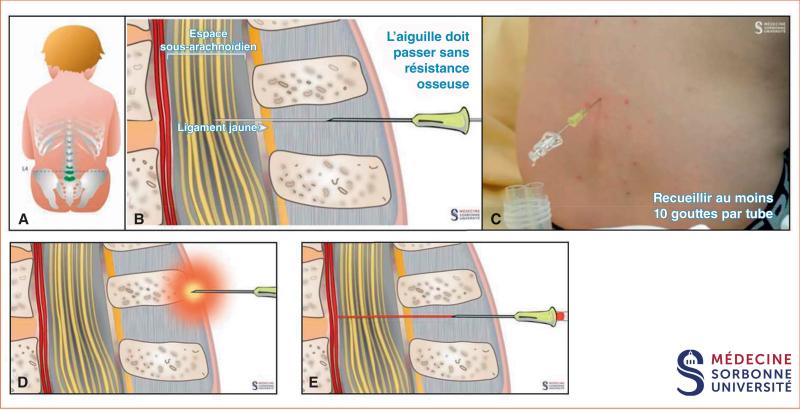
Fig. 37.2. ![]() Ponction lombaire chez l’enfant.
Ponction lombaire chez l’enfant.
A. Positionnement : enfant assis, bas du dos courbé, épaules et hanches parallèles au plan du lit, repère = ligne joignant les crêtes iliaques et le processus épineux L4. B. Insertion de l’aiguille : passage sans résistance osseuse à travers la peau, le tissu sous-cutané, les ligaments supra-épineux puis inter-épineux, le ligament jaune (sensation de ressaut), l’espace péridural, la dure-mère et l’arachnoïde jusqu’à l’espace sous-arachnoïdien. C. Recueil du LCS : 10 gouttes au moins par tube, après retrait de l’aiguille : comprimer le point de ponction puis pansement. D. Échec : butée contre résistance quelques millimètres après passage de la peau = rencontre d’un processus épineux. E. Échec : butée contre résistance plus en profondeur = rencontre du mur vertébral postérieur, risque de PL hémorragique (présence d’un vaste plexus veineux bordant la paroi ventrale de l’espace sous-arachnoïdien) rendant l’interprétation cytologique du LCS difficile.
Source : Extraits de la vidéo « La ponction lombaire en pédiatrie ». Pépite Médecine Sorbonne Université. Auteurs : Dr S. Héritier, Dr M. Kiener, Pr M. Lorrot, A. Caradec, Dr A. Isapof, Dr C. Ravelli, Dr B. Tourniaire, Pr A. Petit. Réalisation : T. Baspeyras. Graphisme : L. Jacquenod.
Poser le diagnostic de méningite
Analyse cytologique :
- nombre de cellules (ou globules blancs) > 5/mm3 = méningite (chez un nouveau-né, ce seuil est à 10/mm3) ;
- attention : un prélèvement traumatique (LCS hémorragique si > 1 000 GR/mm3) peut « faussement » élever la cellularité ; 1 000 GR correspondent à environ 1 élément (ou globule blanc) dans le LCS.
Analyse biochimique :
- protéinorachie (un prélèvement traumatique peut « faussement » élever la protéinorachie) ;
- rapport glycorachie/glycémie ;
- nécessité absolue de doser la glycémie concomitante à la PL ;
- une hypoglycorachie très basse serait un indice de mauvais pronostic ;
- dosage des lactates dans le LCS parfois pratiqué.
Examen microbiologique direct :
- coloration de Gram :
- sensibilité améliorée par concentration du LCS par cytocentrifugation ;
- un inoculum > 105 bactéries/ml est nécessaire pour être visible à l’examen direct ;
- résultat en 30 minutes mais dépendant du germe et de l’opérateur ;
- germe retrouvé :
- cocci à Gram positif en diplocoques : S. pneumoniae ;
- diplocoques à Gram négatif : N. meningitidis ;
- bacilles à Gram négatif polymorphes : H. influenzae ;
- absence de germe au direct :
- origine virale probable ;
- mais interprétation parfois mise en défaut si antibiothérapie préalable.
Culture microbienne (systématique) :
- confirmation de l’identification de la bactérie ;
- étude de l’antibiogramme ;
- évaluation de la CMI du germe aux C3G injectables et à l’amoxicilline.
S’orienter entre méningite bactérienne et méningite virale
Le tableau 37.1 récapitule les caractéristiques d’orientation après étude du LCS.
Tableau 37.1. ![]() Résultats de l’étude du LCS : méningite bactérienne versus méningite virale.
Résultats de l’étude du LCS : méningite bactérienne versus méningite virale.
| LCS | Méningite bactérienne |
|
| Analyse macroscopique |
|
|
| Analyse cytologique |
|
|
| Analyse biochimique |
|
|
| Examen microbiologique direct |
|
|
| Culture microbienne |
|
|
| Autres recherches |
|
|
3. Autres examens biologiques
Hémoculture
Elle est systématique dans le bilan initial et peut isoler une bactérie causale en cas de méningite bactérienne.
Elle ne se substitue pas à l’examen du LCS qui permet à lui seul de porter le diagnostic de méningite.
Autres examens permettant d’identifier l’agent infectieux
Tableau de méningite bactérienne recherche d’une bactérie (hors culture du LCS et hémocultures) :
- si examen microbiologique du LCS négatif (cellularité sans germe) :
- test immunochromatographique BinaxNOW® sur LCS : détecte les molécules de polysaccharides C contenues dans toutes les souches de S. pneumoniae (excellente sensibilité) ;
- PCR pneumocoque ou PCR méningocoque sur le LCS (PCR « classiques » et RT-PCR ou PCR en temps réel, spécifiques d’un agent bactérien) ;
- PCR méningocoque sérique (inutile si > 18 heures après le début du traitement) ;
- PCR méningocoque sur biopsie cutanée de lésion nécrotique en cas de suspicion de méningococcémie ou de purpura fulminans (intérêt majeur si examen du LCS négatif ou impossible).
Tableau de méningite virale → recherche d’un virus, selon les cas :
- dosage de l’interféron α sur LCS augmenté en faveur d’une étiologie virale ;
- PCR entérovirus sur LCS selon orientation ;
- PCR HSV sur LCS en cas de signes encéphalitiques.
Depuis peu, des techniques automatisées de RT-PCR multiplex proposent un diagnostic microbiologique rapide sur un panel élargi d’agents viraux et bactériens responsables d’infections du SNC. Possibilités rares de faux négatifs et de faux positifs.
Autres examens utiles
Bilan inflammatoire orientation vers une cause bactérienne :
- NFS : hyperleucocytose à polynucléaires (mais aucune spécificité) ;
- CRP élevée (utile mais insuffisamment discriminante avec une infection virale) ;
- PCT > 0,5 ng/ml (meilleure que la CRP comme marqueur distinctif entre méningite bactérienne et méningite virale car plus précoce).
L’ionogramme sanguin est surtout utile en cas de réduction de la diurèse afin d’authentifier une complication évolutive de type SIADH (sécrétion inappropriée d’hormone antidiurétique).
La détermination du sérogroupe du méningocoque éventuellement isolé est le complément indispensable pour pouvoir instituer la prophylaxie vaccinale des sujets contacts.
Examens systématiques recommandés : examen du LCS et hémoculture.
Diagnostic de méningite : éléments du LCS > 5/mm3.
Suivre la culture du LCS, même en cas de méningite à liquide clair.
4. Examens d’imagerie
L’imagerie cérébrale n’est pas un examen systématique.
Le scanner cérébral ou, mieux, l’IRM cérébrale est indiqué(e) :
- initialement en cas de :
- signes cliniques évocateurs d’encéphalite : troubles de la conscience variables ou prolongés, convulsions répétées et/ou prolongées, signes de localisation neurologique persistants, modifications durables du comportement ;
- contexte évocateur de méningite bactérienne avec signes évoquant un processus expansif intracrânien et/ou présence de signes d’engagement cérébral (voir supra) ;
- ou plus tard en cas d’évolution défavorable d’une méningite bactérienne, à la recherche d’une complication telle qu’un empyème cérébral ou une thrombose vasculaire.
Pour rappel, cette imagerie (si indiquée initialement) ne doit pas retarder le traitement d’urgence (à débuter ici avant la PL), à savoir l’antibiothérapie intraveineuse et/ou l’aciclovir.
L’échographie transfontanellaire n’a pas d’indication dans ce contexte.
III. Argumenter l’attitude thérapeutique et planifier le suivi
A. Méningite bactérienne
1. Orientation
La prise en charge thérapeutique d’une méningite purulente est une urgence.
La moindre suspicion clinique du diagnostic doit conduire à l’hospitalisation, avec monitoring cardiorespiratoire et pose de voies veineuses périphériques de bon calibre.
L’orientation d’un enfant avec une méningite bactérienne doit être discutée avec le réanimateur pédiatrique et justifie dans tous les cas le rapprochement vers un service de réanimation pédiatrique prévenu de l’état clinique de l’enfant. Si un transfert interhospitalier est nécessaire, il doit être médicalisé (SAMU, SMUR).
Surveillance continue dans les premières heures :
- état hémodynamique ;
- signes d’HTIC sévère : bradycardie, tachycardie, irrégularité du rythme respiratoire
2. Antibiothérapie
Rationnel de prescription
Objectifs de la prise en charge :
- la rapidité d’obtention d’un effet bactéricide dans le LCS ;
- la lutte contre l’inflammation méningée et l’œdème cérébral.
L’antibiothérapie repose sur la prescription d’une C3G injectable (céfotaxime ou ceftriaxone).
Une monothérapie à doses élevées (méningées) est suffisante pour les méningites bactériennes à méningocoque et à pneumocoque.
Le pronostic d’un enfant atteint de méningite bactérienne dépend de la précocité de la mise en route de l’antibiothérapie. Celle-ci doit être débutée dès la réalisation de la PL diagnostique ou même avant si cet examen est contre-indiqué ou à différer.
En pratique, l’antibiothérapie s’impose :
- dès la suspicion diagnostique en cas de signes de détresse vitale (instabilité hémodynamique, signes d’engagement cérébral) lorsque la PL doit être différée ;
- dès la réalisation de la PL ou dès ses premiers résultats (aspect macroscopique, cellularité du LCS, examen microbiologique direct).
Les critères biologiques classiques d’infection bactérienne méningée, tels que l’hypoglycorachie franche avec ratio glucose LCS/sérum < 0,4, l’hyperprotéinorachie (> 0,5 g/l), le syndrome infectieux biologique franc (hyperleucocytose ou leucopénie, élévation de la CRP ou de la PCT), sont utiles pour conforter le diagnostic.
Mais il faut garder en tête qu’aucun signe clinique ou biologique (mis à part l’examen direct) ne permet à lui seul d’affirmer ou d’éliminer l’hypothèse d’une méningite bactérienne. En particulier, aucun marqueur de l’inflammation n’a suffisamment de sensibilité et de spécificité dans ce contexte, même la PCT. En effet, lors d’un épisode infectieux bactérien, la réaction inflammatoire demande un délai et peut rester négative ou peu importante dans les premières heures (12 heures) d’évolution. C’est donc sur un ensemble d’éléments que doit se fonder en urgence la décision thérapeutique.
En cas de doute persistant, le score Meningitest© peut aider le clinicien dans sa décision (sensibilité 100 %, spécificité 51 %).
Une antibiothérapie est indiquée si au moins un des critères suivants est présent en cas de méningite : convulsions, aspect « toxique », purpura, PCT ≥ 0,5 ng/ml, coloration de Gram du LCS positive ou protéinorachie ≥ 0,5 g/l.
Recommandations actuelles
Si le diagnostic de méningite à pneumocoque est suspecté (âge < 1 an, OMA purulente) ou confirmé (cocci à Gram positif à l’examen direct du LCS, BinaxNOW® Streptococcus pneumoniae positif, PCR positive) :
- monothérapie IV : céfotaxime à la dose initiale de 300 mg/kg par jour répartie en quatre injections ;
- adaptation secondaire de l’antibiothérapie selon les résultats de l’antibiogramme (CMI) ;
- durée totale de l’antibiothérapie IV : 10 à 14 jours.
Si le diagnostic de méningite à méningocoque est suspecté (âge ≥ 1 an, contage, purpura) ou confirmé (diplocoque à Gram négatif à l’examen direct du LCS, PCR positive) :
- monothérapie IV : céfotaxime 200 mg/kg par jour répartie en quatre injections (ou ceftriaxone 100 mg/kg par jour) ;
- adaptation secondaire de l’antibiothérapie selon les résultats de l’antibiogramme (CMI) ;
- durée totale de l’antibiothérapie IV : 5 à 7 jours.
Si le diagnostic de méningite à Haemophilus influenzae b est suspecté (bacille à Gram négatif à l’examen direct du LCS, PCR positive) :
- monothérapie IV : céfotaxime 200 mg/kg par jour répartie en quatre injections (ou ceftriaxone 100 mg/kg par jour) ;
- durée totale de l’antibiothérapie IV : 7 jours.
Ces recommandations sont susceptibles de changer en fonction de l’évolution des sérotypes invasifs des pneumocoques chez l’enfant et leur profil de sensibilité aux antibiotiques selon l’efficacité de la politique vaccinale pneumococcique.
3. Autres traitements
Corticothérapie systémique
Les indications de la corticothérapie (dexaméthasone) ont été confirmées par la révision de la conférence de consensus en 2017.
L’efficacité d’une corticothérapie est clairement démontrée au cours des méningites à Haemophilus influenzae b. Elle apporte aussi un bénéfice au cours des méningites à pneumocoque. En cas d’orientation vers un diagnostic de méningite à Haemophilus influenzae b ou à pneumocoque, la prescription de dexaméthasone IV 0,15 mg/kg/6 heures est recommandée de manière simultanée ou au plus tard dans les 12 heures suivant le début de l’antibiothérapie et pendant une durée de 4 jours. En cas de LCS trouble avec examen direct négatif, il faut également la prescrire.
En l’absence d’orientation immédiate bactériologique, elle est indiquée chez le nourrisson de moins de 1 an (prédominance de pneumocoque à cet âge).
Elle est en revanche inutile, mais non délétère, au cours des méningites à méningocoque et doit être arrêtée si elle a été débutée.
Traitements symptomatiques associés
Un traitement antalgique est indispensable pour lutter contre les douleurs, sources d’agitation et d’augmentation de la pression intracrânienne de l’enfant.
Le traitement d’une crise convulsive et la prévention des récidives sont justifiés et font appel aux antiépileptiques conventionnels. Le bénéfice des anticonvulsivants en prévention primaire n’est pas démontré.
Le monitoring de la pression intracrânienne et le traitement de l’œdème cérébral sont discutés selon les équipes et selon les cas.
Orientation initiale de l’enfant à discuter avec un réanimateur pédiatrique.
Antibiothérapie IV de référence : C3G à dose méningée.
Adjonction de dexaméthasone IV : en cas de méningite à pneumocoque ou H. influenzae b (rare).
4. Suivi de l’enfant
Suivi immédiat
Surveillance clinique :
- hémodynamique (FC, TRC, PA) ;
- température : retour à l’apyrexie le plus souvent en 48 heures (chez le nourrisson) ;
- examen neurologique : conscience (Glasgow), mesure du PC (nourrisson).
Réévaluation paraclinique :
- NFS, CRP, PCT : caractère parfois durable du syndrome inflammatoire ;
- suivi du résultat de la culture du LCS et des CMI pour adaptation du traitement antibiotique (choix des molécules et doses).
Imagerie cérébrale (consensus 2017) :
- indiquée en cas d’évolution clinique défavorable ;
- recommandée en cas de méningite à germe inhabituel.
Examen du LCS de contrôle (consensus 2017) :
- inutile le plus souvent en cas d’évolution clinique rapidement favorable ;
- indiqué 48–72 heures après le début du traitement en cas d’évolution clinique défavorable, après imagerie cérébrale si permanence des anomalies neurologiques ;
- recommandé après 48 heures d’antibiothérapie en cas de méningite à pneumocoque avec CMI aux C3G > 0,5 mg/l ou en cas de méningite à germe inhabituel.
Risques pendant la phase initiale d’évolution
Échec de l’antibiothérapie initiale
Une évolution clinique défavorable est définie par la persistance au-delà de 48–72 heures après le début du traitement de : fièvre > 38,5 °C, troubles de conscience, céphalées importantes.
Conduite diagnostique en pratique :
- contrôle des marqueurs infectieux et inflammatoires (NFS, CRP, PCT) ;
- recherche d’une complication (abcès, empyème) : imagerie cérébrale ;
- contrôle de l’examen du LCS avec dosage de la C3G dans le LCS.
Une défaillance hémodynamique peut survenir pendant les premières 24 heures malgré le traitement antibiotique. Cela justifie la surveillance rapprochée en unité de surveillance continue ou en réanimation.
Survenue de complications neurologiques
Principales complications neurologiques en phase aiguë :
- coma, convulsions, état de mal convulsif ;
- paralysies, atteinte des paires crâniennes (en particulier III et VI) ;
- troubles neurovégétatifs : vasomoteurs, hypo- ou hypertension, tachycardie, irrégularités du rythme respiratoire.
Le risque à ce stade est l’engagement cérébral.
Au-delà, la survenue de signes neurologiques nouveaux : augmentation du PC (nourrisson), crises convulsives, anomalies durables de l’examen neurologique, modification de la vision, doit faire rechercher :
- un empyème ;
- une autre complication intracérébrale (hématome sous-dural, accident vasculaire cérébral, hydrocéphalie par blocage de la circulation du LCS) ;
- un syndrome de sécrétion inappropriée d’ADH (SIADH) devant une prise anormale de poids avec hyponatrémie et parfois convulsions.
Suivi à long terme et pronostic
Les méningites bactériennes mettent en jeu le pronostic vital à court terme et le pronostic fonctionnel et séquellaire à plus long terme.
Elles sont à l’origine d’une mortalité élevée dans les pays en développement et demeurent à l’origine de redoutables séquelles neurodéveloppementales et sensorielles dans les pays industrialisés.
La méningite à pneumocoque est la première cause de surdité acquise chez le nourrisson.
Éléments à évaluer au cours du suivi :
- une surdité acquise :
- audiométrie comportementale et potentiels évoqués auditifs (PEA), audiogramme conventionnel (à l’âge où celui-ci est possible) ;
- à J15 de l’épisode aigu, puis tous les 3 mois pendant 1 an ;
- en cas d’hypoacousie précoce : consultation ORL, TDM des rochers et IRM labyrinthique (dépistage d’une ossification intracochléaire susceptible de justifier la mise en place urgente d’implants cochléaires) ;
- un retard de développement psychomoteur et des séquelles motrices ;
- une hydrocéphalie : mesure du PC ;
- une comitialité : survenue ou récidive de crises.
Éléments de mauvais pronostic :
- retard à la mise en route d’un traitement antibiotique bactéricide ;
- âge : nourrisson ;
- germe causal : pneumocoque ;
- gravité du tableau neurologique initial : coma, signes neurologiques de localisation ;
- existence d’un collapsus associé (choc septique) ;
- faible réaction cellulaire, hypoglycorachie, hyperprotéinorachie (LCS).
Un enfant précocement et correctement traité et dont l’examen neurologique s’est rapidement normalisé au décours de la phase aiguë, peut être habituellement considéré comme préservé de séquelles tardives, avec une incertitude cependant vis-à-vis de l’éventualité de séquelles cognitives.
Une infection sévère et invasive (donc une méningite) à bactéries encapsulées (pneumocoque, méningocoque et H. influenzae b), même au terme d’un épisode unique, doit conduire à une exploration de l’immunité (voir chapitre 26).
Une méningite bactérienne récidivante (pneumocoque) ou atypique par l’âge ou le germe retrouvé doit faire rechercher systématiquement une brèche méningée.08
Suivi immédiat : fièvre, examen neurologique (PC), ± bilan inflammatoire.
Évolution clinique défavorable imagerie cérébrale et contrôle de l’examen du LCS.
Suivi systématique du risque de surdité acquise.
5. Mesures préventives
Qui cibler ?
L’identification des sujets contacts est utile dans certaines situations.
Les bactéries responsables des méningites purulentes proviennent du nasopharynx et sont ainsi susceptibles d’être diffusées à l’entourage. Toutefois le risque de cas secondaires ne concerne essentiellement que le méningocoque.
Actions pour réduire la survenue de cas secondaires (selon les bactéries) :
- antibioprophylaxie des sujets contacts (méningocoque quel que soit son sérogroupe) ;
- vaccination des sujets contacts (méningocoque A, C, W ou Y) ;
- déclaration obligatoire (infections invasives à méningocoque).
Sont inutiles : l’éviction de la collectivité des sujets contacts (par exemple, éviction scolaire de la fratrie), la désinfection ou la fermeture d’un établissement scolaire fréquenté par le malade.
Méningite à méningocoque
Isolement en milieu hospitalier
Il s’agit d’un isolement de type « gouttelettes » pendant les 24 premières heures de traitement pour éviter la contagion. Au-delà, la poursuite de l’isolement en chambre seule se justifie pour garantir la tranquillité du patient (bruit, lumière).
Antibioprophylaxie des sujets contacts
Objectifs de l’antibioprophylaxie :
- réduire le risque de survenue de cas secondaires précoces (< 10 jours) en éliminant le portage chez les sujets exposés aux sécrétions oropharyngées de l’enfant atteint ;
- prévenir la diffusion dans la population d’une souche pathogène par des porteurs sains.
Le risque de survenue d’une infection invasive méningococcique (IIM) est multiplié par 800 chez les sujets contacts d’une IIM par rapport au taux de base de la population.
Les sujets contacts sont ainsi définis : personnes exposées aux sécrétions oropharyngées du sujet infecté dans les 10 jours précédant son admission, donc essentiellement l’entourage familial du cas, la crèche, les camarades de classe et de jeu. Dans les autres circonstances, l’évaluation du risque doit prendre en compte : la proximité (distance < 1 mètre), le type de contact (face à face), la durée (> 1 heure, sauf contact bouche à bouche).
Modalités pratiques :
- administration précoce :
- dans les 24–48 heures suivant le diagnostic d’IIM ;
- aucune utilité au-delà de 10 jours après le dernier contact avec le malade ;
- molécule de choix = rifampicine par voie orale pendant 2 jours :
- nouveau-né : 5 mg/kg/12 heures ; nourrisson et enfant : 10 mg/kg/12 heures ; adulte : 600 mg/12 heures ;
- en informant de la coloration orange des urines et des sécrétions lacrymales (porteurs de lentilles de contact) et de l’interaction avec l’activité des contraceptifs oraux.
Vaccination ciblée autour d’un cas
Une prophylaxie vaccinale est parfois possible.
Elle complète l’antibioprophylaxie lorsque la souche de méningocoque responsable est d’un sérotype vis-à-vis duquel existe un vaccin polyosidique conjugué approprié.
Elle est réalisée de manière concomitante à l’antibioprophylaxie, selon les mêmes conditions (définition des sujets contacts, délai maximal de 10 jours) chez les sujets non vaccinés ou ceux dont la vaccination remonte à plus de 3 ans pour un vaccin non conjugué et plus de 5 ans pour un vaccin conjugué.
Son objectif est d’éviter les cas secondaires tardifs (> 10 jours) liés à la circulation persistante de la souche virulente dans la communauté au-delà de la période couverte par l’antibioprophylaxie.
Dans le cadre de la vaccination autour d’un cas, seule la vaccination polyosidique conjuguée contre les méningocoques des sérogroupes A, C, Y et W est recommandée :
- vaccin méningococcique C conjugué monovalent en cas d’IIM du sérogroupe C ;
- vaccin tétravalent conjugué (ou A/C/Y/W) en cas d’IIM liée à l’un de trois autres sérogroupes (essentiellement W et Y, le sérogroupe A étant exceptionnel en France) ;
- chez les enfants âgés de plus de 6 semaines ou 1 an selon les AMM respectives des vaccins.
La vaccination contre le sérogroupe B (vaccin protéique Bexsero®) majoritaire en France (deux tiers des cas) n’est pas recommandée autour des cas sporadiques en France. Elle est réservée aux situations particulières (grappes de cas et épidémies).
Déclaration obligatoire
L’infection invasive à méningocoque est une pathologie infectieuse à déclaration obligatoire.
Le signalement doit être effectué sans délai auprès de l’ARS.
Cette procédure permet à l’ARS d’identifier les sujets contacts, d’évaluer les mesures de prophylaxie, d’organiser leur mise en œuvre et de s’assurer qu’elles sont effectives.
Les signalements transmis à l’ARS sont ensuite dirigés vers l’InVS pour le suivi épidémiologique.
Méningite à méningocoque :
- isolement dès que possible ;
- antibioprophylaxie des sujets contacts par rifampicine per os ;
- vaccination post-exposition indiquée qu’en cas d’IMM de sérogroupe C, A, W ou Y ;
- déclaration obligatoire.
Autres méningites
Méningite à pneumocoque
Les méningites à pneumocoque ne sont pas épidémiques.
Aucune action spécifique n’est nécessaire :
- isolement « gouttelettes » non recommandé ;
- aucune antibioprophylaxie, même chez les sujets non ou mal vaccinés ;
- poursuite du calendrier vaccinal (vaccin pneumococcique conjugué à 13 valences) chez le sujet malade et son entourage (s’il relève de la vaccination), sans délai particulier ;
- pas de déclaration obligatoire.
Méningite à Haemophilus influenzae b
Il n’existe pas de recommandation officielle en France.
Mesures préventives à envisager :
- isolement recommandé pendant les premières 24 heures de traitement d’après l’Académie américaine de pédiatrie (Red Book, 2009) ;
- antibioprophylaxie chez l’enfant malade en relais du traitement curatif discutée (rifampicine pendant 4 jours) : elle est considérée comme nécessaire en cas de vaccination incomplète chez les sujets contacts âgés de moins de 4 ans ;
- poursuite du calendrier vaccinal le cas échéant chez le sujet malade et les sujets de son entourage âgés de moins de 5 ans et non ou incomplètement vaccinés ;
- pas de déclaration obligatoire.
Méningite à pneumocoque : aucune mesure prophylactique pour les sujets contacts.
B. Méningite virale
1. Prise en charge thérapeutique
L’hospitalisation n’est pas systématique. Une prise en charge ambulatoire est possible en cas de forme bénigne, en l’absence d’hésitation diagnostique avec une méningite bactérienne ou une encéphalite.
Aucune mesure d’isolement spécifique n’est recommandée.
En cas d’orientation très évocatrice de méningite virale commune :
- traitement symptomatique : repos, antalgiques, hydratation, antiémétiques ;
- surveillance clinique.
Au moindre doute :
- hospitalisation ;
- possible méningite bactérienne : antibiothérapie probabiliste IV selon l’âge ;
- suspicion d’encéphalite associée (voir les données cliniques évocatrices ci-après) : aciclovir IV.
Seul l’examen du LCS permet d’exclure le diagnostic de méningite bactérienne.
2. Suivi de l’enfant
Le suivi immédiat est avant tout infectieux et neurologique.
L’apyrexie est obtenue en moins de 7 jours, souvent en moins de 48 heures pour les méningites à entérovirus. Le contrôle du LCS est alors inutile.
Le pronostic est habituellement bon, sans dépistage systématique ultérieur.
Méningo-encéphalites
I. Pour bien comprendre
Les encéphalites désignent une atteinte du parenchyme cérébral. Elles sont fréquemment associées à une réaction inflammatoire, volontiers modérée, du LCS (méningo-encéphalite).
Les méningo-encéphalites infectieuses partagent des causes virales identiques à celles des méningites virales (entérovirus essentiellement et HHV6, virus de la varicelle et du zona, virus EBV ou virus ourlien). Il peut exister ainsi un continuum entre un tableau de méningite de type viral isolé et un tableau évocateur de méningo-encéphalite.
On distingue :
- l’encéphalite consécutive à une réplication virale active au sein du parenchyme cérébral (typiquement la méningo-encéphalite herpétique) ;
- et l’encéphalite dite « post-infectieuse » ou « inflammatoire », communément appelée encéphalomyélite aiguë disséminée (ou ADEM, Acute Disseminated Encephalomyelitis).
Ces formes ADEM sont les plus fréquentes et l’on considère que l’agent infectieux initial, le plus souvent viral, a induit lors de son passage transitoire une réaction inflammatoire au sein du parenchyme cérébral de l’hôte, qui devient pathologique et est responsable de l’encéphalite. L’agent déclencheur n’est alors plus présent et n’est d’ailleurs, le plus souvent, pas identifié. Ce mécanisme explique pourquoi, dans ces formes, ce sont surtout les médicaments anti-inflammatoires (corticoïdes notamment) qui s’avèrent efficaces plutôt que les antiviraux.
Agents pathogènes impliqués dans les méningo-encéphalites :
- HSV (pas le plus fréquent mais à évoquer en premier lieu en raison de sa gravité et de l’urgence thérapeutique antivirale) ;
- VZV, entérovirus, adénovirus, HHV6, grippe, EBV, CMV ;
- certaines bactéries : Lyme, mycoplasme, Bartonella henselae (griffes du chat), Listeria, BK ;
- autres agents infectieux en fonction du contexte, notamment : Plasmodium falciparum (neuropaludisme), VIH, virus chikungunya.
D’autres causes non infectieuses peuvent être responsables d’encéphalite aiguë chez l’enfant, en particulier auto-immunes ou dysimmunitaires.
Elles devront systématiquement être discutées si l’étiologie infectieuse ne se confirme pas.
II. Diagnostic
A. Enquête clinique
Données cliniques évocatrices d’une atteinte encéphalitique :
- troubles variables de la conscience, fluctuants ou prolongés (voir chapitre 68) ;
- crises convulsives (parfois état de mal épileptique) ;
- modifications du comportement, troubles mnésiques et/ou du langage ;
- signes de localisation neurologique focaux, syndrome pyramidal ;
- troubles de l’équilibre, atteinte des paires crâniennes ;
- troubles hémodynamiques.
Bien que peu spécifiques et parfois même d’évolution fluctuante au début, un ou plusieurs de ces signes associés à une fièvre doivent absolument faire suspecter une encéphalite.
L’étiologie herpétique doit être évoquée en premier et conduire à la prescription en urgence d’aciclovir IV, avant même tout
Tableau clinique d’encéphalite aciclovir IV en urgence.
B. Enquête paraclinique
1. Examen du LCS
Analyses macroscopique, cytologique et biochimique :
- en cas de méningo-encéphalite herpétique : liquide clair avec pléiocytose modérée à prédominance lymphocytaire et hyperprotéinorachie modérée (mais le LCS peut être normal en cas d’encéphalite isolée) ;
- en cas d’encéphalite post-infectieuse : liquide clair avec cellularité modérément élevée voire normale, surtout au début de l’évolution.
Autres examens sur le LCS susceptibles d’argumenter l’étiologie :
- PCR HSV (indispensable) et dosage d’interféron ;
- et selon le contexte (PCR, principalement) :
- VZV, entérovirus, adénovirus, HHV6, grippe, EBV, CMV, VIH, chikungunya ;
- Lyme, mycoplasme, Bartonella henselae (griffes du chat), Listeria, BK.
2. Examens d’imagerie
L’imagerie cérébrale est indispensable en cas de signes évocateurs d’encéphalite, ne faisant différer la PL qu’en cas d’HTIC menaçante ou suspicion de processus expansif intracrânien.
Elle ne doit pas pour autant retarder l’instauration du traitement probabiliste par aciclovir IV, qui doit ainsi être commencé avant même l’imagerie cérébrale (et donc la PL).
Au cours de l’encéphalite herpétique, l’IRM cérébrale peut montrer précocement des hypersignaux souvent bilatéraux et asymétriques des lobes temporaux en pondération T2 et FLAIR (fig. 37.3).
Dans les formes post-infectieuses (ADEM), l’IRM peut montrer des hypersignaux de la substance blanche (et/ou grise), le plus souvent bilatéraux et asymétriques. L’aspect des lésions n’est corrélé ni avec la sévérité clinique ni avec le pronostic évolutif.
Une IRM normale n’élimine pas le diagnostic d’encéphalite.
L’IRM doit être préférée au scanner, moins sensible et plus tardif.
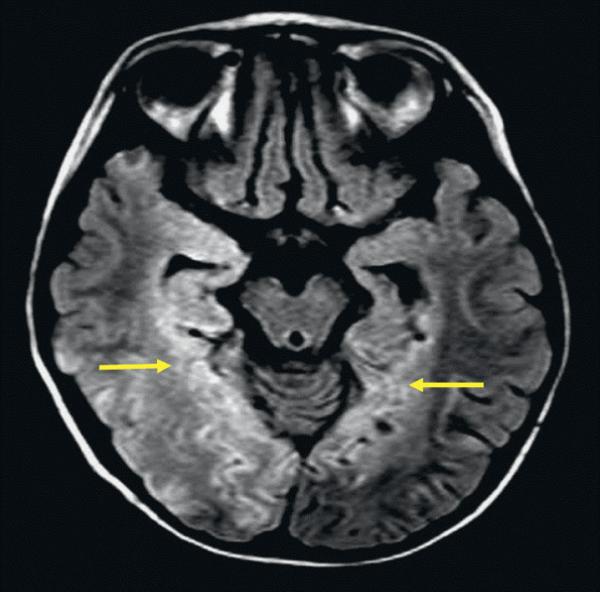
Fig. 37.3. ![]() Lésions IRM d’encéphalite herpétique.
Lésions IRM d’encéphalite herpétique.
IRM cérébrale. Coupe axiale passant par les pédoncules cérébraux en pondération FLAIR. Hypersignal temporal bilatéral prédominant à droite.
3. Électroencéphalogramme (EEG)
L’EEG peut mettre en évidence un tracé évocateur d’encéphalite : aspect ralenti avec parfois des ondes lentes périodiques et/ou des pointes-ondes frontotemporales.
Un EEG normal n’élimine pas le diagnostic d’encéphalite.
Examens pour argumenter le diagnostic d’encéphalite : LCS, IRM cérébrale, EEG.
III. Prise en charge thérapeutique et suivi de l’enfant
A. Prise en charge thérapeutique
L’hospitalisation est indispensable.
Mesures thérapeutiques urgentes :
- monitoring cardiorespiratoire, voies veineuses périphériques ;
- traitement antiviral probabiliste : aciclovir 500 mg/m2/8 heures IV ;
- traitement symptomatique : antipyrétiques, antiépileptiques si convulsions.
Dans les formes graves en réanimation :
- mesures générales chez l’enfant comateux : ventilation mécanique si Glasgow < 8, etc. ;
- traitement de l’HTIC éventuelle (posture, ventilation, mannitol).
Aucun examen paraclinique ne doit retarder la mise en route de l’aciclovir IV.
Ce traitement pourra être arrêté en cas de négativité d’au mieux deux PCR HSV dans le LCS à 48 heures d’intervalle. Dans le cas contraire, il doit être poursuivi pendant 15 à 21 jours.
B. Suivi de l’enfant
Le suivi immédiat est avant tout infectieux et neurologique.
Un suivi des éventuelles séquelles à distance (cognition, comportement, vision, audition) est indispensable.
Le pronostic d’une encéphalite est difficile à prévoir. Dans les formes post-infectieuses, la guérison sans séquelles n’est pas rare, de manière spontanée ou après un traitement anti-inflammatoire s’il s’avère nécessaire.
Le pronostic d’une méningo-encéphalite herpétique est fonction avant tout de la précocité du traitement par aciclovir IV. La mortalité à la phase aiguë est élevée. Le risque de séquelles cognitives est également important.
Références

|
SPILF. Prise en charge des méningites bactériennes aiguës communautaires. Texte court. 2017. Médecine et Maladies Infectieuses 2019;49(6):367–98. https://www.sciencedirect.com/science/article/pii/S0399077X18300416?via… |

|
Ponction lombaire chez l’enfant. Pépite Médecine Sorbonne Université. Auteurs : Dr S. Héritier, Dr M. Kiener, Pr M. Lorrot, A. Caradec, Dr A. Isapof, Dr C. Ravelli, Dr B. Tourniaire, Pr A. Petit. Réalisation : T. Baspeyras. Graphisme : L. Jacquenod. https://www.youtube.com/watch?v=jhRlIO4LDOQ |
