
ITEM 258 Élévation de créatininémie
- Connaître la formule de Schwartz chez l'enfant.
ITEM 264 Insuffisance rénale chronique chez l'adulte et l'enfant
- Définir le stade d'une maladie rénale chronique.
- Connaître les facteurs de progression des maladies rénales chroniques et les mesures thérapeutiques adaptées.
- Diagnostiquer les complications des maladies rénales chroniques et connaître le principe de leur traitement.
- Connaître les modalités des traitements de suppléance de l'insuffisance rénale terminale.
ITEM 348 Insuffisance rénale aiguë. Anurie
- Diagnostiquer une IRA et sa sévérité (oligurie, anurie) chez l'adulte et l'enfant.
- Savoir analyser une élévation de la créatininémie en fonction du contexte clinique, de la notion de créatininémie antérieure et grader la sévérité en tenant compte de la créatininémie et de la diurèse, savoir diagnostiquer une IRA d'une IRC, reconnaître une IRA sur IRC.
- Connaître les principales causes d'IRA chez l'enfant (SHU, déshydratation, choc, etc.) et les mesures hygiéno-diététiques de prévention des SHU.
La créatininémie est plus basse chez l'enfant que chez l'adulte.
On utilise la formule de Schwartz pour évaluer le débit de filtration glomérulaire (DFG) chez l'enfant.
Les grandes causes d'insuffisance rénale aiguë (IRA) et de maladie rénale chronique (MRC) sont les mêmes que chez l'adulte, mais leur épidémiologie est différente.
La première cause d'IRA chez l'enfant âgé de moins de 3 ans est le syndrome hémolytique et urémique (SHU) typique.
Les causes principales de MRC de l'enfant sont les hypodysplasies rénales, les uropathies et les maladies génétiques.
La MRC est en rapport avec une réduction congénitale ou acquise du nombre de néphrons avec ou sans altération du débit de filtration glomérulaire (DFG).
Ses deux risques majeurs sont la progression vers l'insuffisance rénale chronique puis terminale dans l'enfance, et la mortalité cardiovasculaire à l'âge adulte.
I. Pour bien comprendre
Le rein a de multiples fonctions qui comprennent l'homéostasie et l'équilibre du volume du compartiment extracellulaire, l'équilibre acidobasique, l'équilibre phosphocalcique, le métabolisme osseux et somatotrope ainsi que la production des globules rouges.
Chez l'enfant, la créatininémie augmente avec l'âge (tableau 48.1).
À la naissance, la créatininémie est celle de la mère (environ 80 μmol/l), puis elle diminue jusqu'à 20 à 30 μmol/l à 1 semaine de vie et réaugmente avec l'âge et la masse musculaire.
| Jusqu'à 5 ans | < 35 μmol/l |
|---|---|
| 6 à 10 ans | < 50 μmol/l |
| Après la puberté | < 90 μmol/l |
Le débit de filtration glomérulaire (DFG) est le même que celui de l'adulte à partir de l'âge de 2 mois. Il est exprimé en ml/min/1,73 m2.
Il est estimé chez l'enfant par la formule de Schwartz (révisée en 2019) :
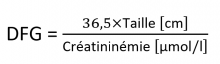
II. Insuffisance rénale aiguë
A. Diagnostic
L'insuffisance rénale aiguë est définie par une altération de la fonction rénale < 3 mois : élévation de la créatininémie, diminution du DFG et/ou oligurie ou anurie (inconstantes en pédiatrie).
1. Signes d'appel
Évoquer une IRA :
- oligurie ou anurie ;
- nausées, vomissements ;
- pâleur (anémie) ;
- signes de surcharge hydrosodée : œdèmes, HTA, voire œdème aigu pulmonaire (OAP), insuffisance cardiaque, convulsions ;
- complications des troubles ioniques : hyperkaliémie (paresthésies, troubles du rythme mettant en jeu le pronostic vital), hypocalcémie (paresthésies, fasciculations, tétanie, signes de Chvosteck et de Trousseau), acidose métabolique (dyspnée de Kussmaul).
Lors de la découverte d'une insuffisance rénale, certains éléments permettent d'orienter vers une IRC plutôt que vers une IRA :
- cassure staturo-pondérale ;
- polyuropolydipsie ancienne, énurésie ;
- créatininémie antérieure élevée ;
- anémie ;
- hypocalcémie ;
- petits reins sur l'échographie anténatale et/ou postnatale ;
- signes osseux d'hyperparathyroïdie ;
- HTA.
2. Orientation diagnostique
IRA fonctionnelle, ou « pré-rénale » (baisse de la perfusion rénale)
- Caractéristiques : urines concentrées avec urée urinaire/urée plasmatique > 10.
- Évaluer : hydratation et volémie, prise de néphrotoxiques.
- Causes : hypovolémie (déshydratation, hypotension, choc, troisième secteur, hémorragie), pathologie vasculaire ou toxique ou iatrogène (par exemple, AINS, diurétiques).
- Prise en charge : restauration de la volémie et/ou arrêt du médicament en cause.
IRA parenchymateuses
- Caractéristiques : IRA organique avec urée urinaire/urée plasmatique < 10.
- Causes :
- nécrose tubulaire aiguë : diurèse variable, protéinurie tubulaire (< 1 g/l, protéines de bas poids moléculaire) ;
- néphrites tubulo-interstielles aiguës (toxiques, immunoallergiques, infectieuses) : signes généraux, protéinurie tubulaire, leucocyturie, ± éosinophilurie, éosinophilie ;
- glomérulonéphrites aiguës :
- post-infectieuses : infection récente à streptocoque A ou staphylocoque, syndrome néphritique : œdèmes voire OAP, HTA, IRA organique, hématurie glomérulaire marron sans caillot ni douleur, protéinurie glomérulaire (> 1 g/l, albumine) ; diagnostic : C3 effondré puis normalisation dans les 2 mois ;
- purpura rhumatoïde, néphropathie à IgA (Berger), lupus… ;
- syndrome hémolytique et urémique.
IRA post-rénales (obstruction bilatérale ou sur rein unique)
- Évaluer : présence d'un globe, d'un contact lombaire.
- Diagnostic : échographie rénale et des voies urinaires.
B. Points clés sur le syndrome hémolytique et urémique typique
1. Généralités
Le syndrome hémolytique et urémique (SHU) typique est le SHU post-diarrhéique secondaire à une infection à E. coli producteur de shigatoxine (STEC) ou plus rarement à Shigella dysenteriae.
Il s'agit de la première cause d'IRA avant l'âge de 3 ans, avec une centaine de cas par an en France.
Il existe une mortalité de 1 à 2 % et une évolution vers la MRC dans 30 % des cas.
2. Diagnostic
Triade biologique :
- anémie hémolytique mécanique : anémie pour l'âge, haptoglobine effondrée, bilirubine libre et LDH élevées, schizocytes > 2 % (Coombs négatif) ;
- thrombopénie (< 150 G/l) ;
- IRA organique.
Signes cliniques :
- prodromes digestifs : diarrhées glairo-sanglantes fréquentes, vomissements, douleurs abdominales survenant quelques jours avant le SHU ;
- phase d'état de début brutal avec triade biologique du SHU : pâleur ± ictère, oligo-/anurie (50 % des enfants), hématurie et protéinurie glomérulaires, HTA ;
- atteintes extrarénales plus rares : atteinte du système nerveux central (déficit neurologique), digestive (pancréatite, colite, etc.), hépatique, cardiaque ; convulsions secondaires à l'atteinte neurologique, à l'HTA ou aux désordres électrolytiques.
Examens complémentaires :
- diagnostiques : NFS-plaquettes, recherche de schizocytes, haptoglobine, bilirubine, LDH, urée, créatinine, ionogramme sanguin, albuminémie, protéinurie, hématurie ;
- préthérapeutiques : bilan prétransfusionnel ;
- étiologiques : recherche de la bactérie sécrétrice de shigatoxine par analyse de selles ou écouvillonnage rectal, culture et détection par PCR des shigatoxines ;
- retentissement (atteintes extrarénales) : bilans pancréatique et hépatique, troponine et ECG ; IRM cérébrale si symptomatologie neurologique ;
- à visée de diagnostic différentiel (pour rechercher un SHU atypique) : étude du complément, dosage de l'ADAMTS13.
3. Prise en charge thérapeutique et suivi
Hospitalisation en milieu spécialisé.
Pas de traitement étiologique du SHU.
Traitement symptomatique :
- maintien d'une euvolémie ;
- éviter les apports potassiques ;
- traitement de l'HTA et des troubles hydroélectrolytiques ;
- épuration extrarénale si : oligo-/anurie prolongée, surcharge hydrique, hyperkaliémie et/ou acidose menaçantes ;
- transfusion de CGR si anémie mal tolérée.
Traitements non recommandés sauf exception :
- pas de transfusion de plaquettes (risque de surcharge, de majoration de la MAT, d'immunisation anti-HLA ; efficacité limitée à quelques heures) sauf saignement actif ;
- pas d'antibiothérapie à large spectre sauf sepsis sévère ;
- pas de ralentisseurs du transit.
Suivi régulier :
- surveillance annuelle de la BU et de la PA ;
- néphroprotection pour tous (voir § III.C) ;
- IEC en cas de protéinurie et/ou d'HTA.
4. Prévention
Mesures de prévention à diffuser :
- pas de laitages non pasteurisés ni de viande bovine peu cuite avant l'âge de 3 ans ;
- éviction du contact avec les bovins/ovins et leur environnement avant l'âge de 3 ans ;
- lavage des fruits et légumes, consommation d'eau traitée ;
- lavage des mains avant de préparer le repas et en sortant des toilettes, lavage des ustensiles de cuisine ;
- en cas de gastroentérite aiguë : éviction de baignades dans les lieux publics.
Mesures administratives :
- déclaration des cas de SHU à Santé Publique France ;
- et déclaration obligatoire de toxi-infection alimentaire en cas de cas groupés.
Mesures de prévention à retenir.
III. Maladie rénale chronique
A. Généralités
La maladie rénale chronique (MRC) est définie par la présence, pendant plus de 3 mois, de marqueurs d'atteinte rénale : anomalies morphologiques, histologiques et/ou biologiques (protéinurie, albuminurie, hématurie, leucocyturie, DFG < 60 ml/min/1,73 m2).
Elle est classée en stades de sévérité croissante selon le niveau de DFG (tableau 48.2).
Le stade 1 est équivalent à une fonction rénale normale. Il correspond à toutes les situations de réduction néphronique sans modification du DFG.
| Stade | DFG (ml/min/1,73 m2) |
|---|---|
| 1 | ≥ 90 |
| 2 | 60–89 |
| 3 | 30–59 |
| 4 | 15–29 |
| 5 | < 15 |
B. Diagnostic
Situations à risque nécessitant un dépistage de la MRC :
- antécédent de prématurité, de retard de croissance intra-utérin ;
- antécédent de cancer, de cardiopathie, obésité, maladie de système, maladie chronique ;
- néphropathie, uropathie, traitement néphrotoxique.
Causes de MRC de l'enfant :
- anomalies congénitales du rein et des voies urinaires : hypodysplasies rénales et uropathies (50 à 60 % des cas) ;
- néphropathies acquises glomérulaires (5 à 15 %) ou interstitielles ;
- néphropathies héréditaires (10 à 20 %).
Dépistage :
- mesure de la PA : tous les ans chez les enfants de plus 3 ans, à chaque consultation dans les situations à risque de MRC quel que soit l'âge, dans de bonnes conditions (au repos, brassard adapté) ;
- recherche de protéinurie par bandelette urinaire : dépistage chez tout enfant recommandé par la médecine scolaire lors de l'entrée au CP (6 ans) et en classe de 6e (11 ans), tous les ans dans les situations à risque de MRC.
Évoquer une MRC devant :
- retard de croissance, polyuropolydipsie (réveils nocturnes pour boire ± énurésie), déformations osseuses mal expliquées ;
- HTA : majorité des HTA chez l'enfant = secondaire ; faire un bilan étiologique extensif en cas d'HTA avérée (voir chapitre 50).
Dépistage : mesure de la PA et de la protéinurie par bandelette urinaire.
C. Principes de la prise en charge de la MRC
Les facteurs de progression de la MRC (HTA, protéinurie, néphrotoxiques, infections, facteurs de risque cardiovasculaire…) seront pris en charge comme chez l'adulte.
La néphroprotection repose sur un régime équilibré sans excès de protéines animales ni de sel, la pratique régulière du sport, l'éviction des médicaments néphrotoxiques (AINS), l'adaptation des doses de médicaments à la fonction rénale, la mise à jour des vaccinations (dont celle contre l'hépatite B), ainsi que la prévention du capital vasculaire et la protection du bras non dominant en vue de la création d'une fistule artérioveineuse.
La prise en charge de la MRC en pédiatrie tient compte d'un indicateur spécifique : la vitesse de croissance staturale. Le retard de croissance et le retard pubertaire secondaires à la MRC doivent être pris en charge précocement, avant la greffe.
Cela nécessite de contrôler plusieurs paramètres : l'hydratation extracellulaire, l'équilibre acidobasique, les apports caloriques et la nutrition, l'équilibre phosphocalcique et vitaminique, l'anémie, l'hormone de croissance.
Le traitement symptomatique de l'insuffisance rénale chronique (correction de la déshydratation, de l'acidose et de l'anémie, prévention de l'ostéodystrophie rénale et optimisation des apports nutritionnels) devra être optimisé avant l'instauration du traitement par hormone de croissance recombinante et sera maintenu pendant toute la durée du traitement.
Le traitement de suppléance de la fonction rénale fait appel aux mêmes techniques que chez l'adulte. La transplantation rénale est le meilleur traitement de la MRC de l'enfant et doit être privilégiée.
Le suivi de la MRC est multidisciplinaire et individualisé.
La MRC doit être surveillée à vie même si le DFG est normal lors de l'évaluation initiale. À l'autre extrême, cette surveillance ne s'arrête pas avec la transplantation rénale.
La surveillance du développement psychologique et social de l'enfant, l'adaptation au rythme scolaire et l'encadrement éducatif sont nécessaires pour donner la meilleure chance de développement scolaire et professionnel aux malades pédiatriques avec handicap rénal.
La très grande majorité des enfants ayant une MRC parvient à l'âge adulte. La transition correspond à la période de passage d'une prise en charge pédiatrique vers une prise en charge adulte pour de jeunes patients atteints de pathologies chroniques. Ce processus doit être bien organisé et structuré, afin d'éviter le risque de rupture du suivi médical et réduire celui des complications de la maladie chronique.
Références
Pietrement C., Allain-Launay E., Bacchetta J., et al. Diag¬nostic et prise en charge de la maladie rénale chronique de l'enfant : recommandations de la Société de néphrologie pédiatrique (SNP). Arch Pediatr, 2016;23(11):1191–200. Références Pietrement C., Allain-Launay E., Bacchetta J., et al. Diag¬nostic et prise en charge de la maladie rénale chronique de l'enfant : recommandations de la Société de néphrologie pédiatrique (SNP). Arch Pediatr, 2016;23(11):1191–200.
